原创精选> 正文
药闻头条 | 辉瑞新冠口服药拟进军欧盟!BioNTech癌症疫苗获快速通道资格
2021-11-22 14:08
- 辉瑞(PFE) 0
- 默沙东(MRK) 0
- Moderna(MRNA) 0
I 辉瑞拟向欧盟申请新冠口服药物授权,旗下新冠加强针获批
据悉,辉瑞拟向欧盟申请授权其新冠药物Paxlovid,欧洲药品管理局昨日表示,目前正在审查辉瑞新冠口服药Paxlovid的使用数据,以便提供建议。德国卫生部发言人也表示:“本国卫生部正在与辉瑞就可能采购新冠药物Paxlovid进行接触。”

另外,美国食品药品监督管理局(FDA)上周已批准Moderna $MRNA 和辉瑞 $PFE 的新冠疫苗加强针用于所有成年人,加强针使用要等到美国疾病控制和预防中心(CDC)签字后才能生效。
I 君实生物今日大涨!旗下第二款新冠中和抗体获批临床
君实生物 $01877.HK 今日一度大涨逾6%,昨日发布公告称旗下JS026注射液临床试验申请获药监局批准,用于新型冠状病毒肺炎(COVID-19)的预防和治疗。

据了解,JS026注射液是一种重组全人源单克隆抗体,主要用于COVID-19的预防和治疗。进入临床试验后,JS026与君实生物的首款中和抗体药物埃特司韦单抗(etesevimab,JS016)具有联合用药的潜力,以有效应对各种病毒突变。
I mRNA癌症疫苗获得FDA快速通道资格,治疗黑色素瘤
2021年11月19日,BioNTech $BNTX 公司宣布,美国FDA已授予BNT111快速通道资格。BNT111是一款治疗性mRNA癌症疫苗,目前正在进行一项2期临床试验。

快速通道资格(FTD)旨在加速针对严重疾病的药物开发和快速审查,在研药物获得快速通道资格,意味着药企在研发阶段可以与FDA进行更频繁的互动,在提交上市申请后如果符合相关标准则有资格进行加速审批和优先审查。
I 和黄医药1类新药获批临床,下月公布两款产品临床数据
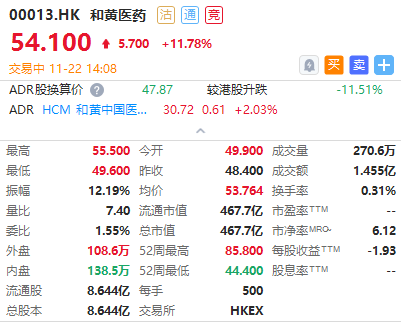
和黄医药 $00013.HK 今日大涨近12%,中国国家药监局药品审评中心(CDE)数据显示,上周有12款1类新药获得临床试验默示许可,和黄医药1类新药HMPL-653胶囊在列,用于治疗晚期恶性实体瘤及腱鞘巨细胞瘤
另外,和黄医药于公告称,公司将于12月11日至14日举行的第63届美国血液学会(ASH)年会上发表HMPL-523及HMPL-306 进行中的临床研究的最新分析与更新。HMPL-523是一种研究性小分子靶向脾酪氨酸激酶(Syk)的口服抑制剂。
风险及免责提示:以上内容仅代表作者的个人立场和观点,不代表华盛的任何立场,华盛亦无法证实上述内容的真实性、准确性和原创性。投资者在做出任何投资决定前,应结合自身情况,考虑投资产品的风险。必要时,请咨询专业投资顾问的意见。华盛不提供任何投资建议,对此亦不做任何承诺和保证。
推荐文章
一周财经日历 | AI海啸来袭!英伟达GTC叠加“亚洲最大AI科技展”ComputeX登场!5月大小非农即将披露;美团财报压轴出场
港股周报 | 5月收官!华为“韬定律”引爆半导体;从暴涨23%到跳水,智谱上演“天地板”式震荡;泡泡玛特大涨,段永平日赚10亿
美股机会日报 | 戴尔盘前狂飙34%!大幅上调全年业绩指引;字节拟采购数百万颗高通AI ASIC芯片;太空概念突发利空,盘前集体回落
一周IPO | 赚到手软!四只新股齐大涨,深演智能首日狂飙超265%;SpaceX、Anthropic再传大消息!
打新攻略 | 中签即赚1.7万港元?深演智能三日暴涨逾700%!天辰生物等火热招股中,下一只爆款新股是谁?
华盛早报 | 美伊据悉再延长休战60天!Anthropic H轮估值9650亿美元反超OpenAI;戴尔AI收入暴增,绩后飙升近40%
5月29日外盘头条:Anthropic新一轮融资后估值达9650亿美元 机构料美伊达成协议概率较高
一图看懂 | 小鹏汽车Q1营收同比下降17.6%,Q2交付和营收预期强劲,预计Robotaxi、人形机器人年内实现量产

