原创精选> 正文
药闻头条丨超3亿美元!美国加购礼来君实新冠抗体,赛生再获肿瘤药独家权益
2021-09-17 14:02
I 3.3亿美元订单!美国政府追加采购君实/礼来新冠抗体「埃特司韦单抗(JS016)」
礼来昨日(9月16日)宣布,美国政府额外购买其授权紧急使用的中和抗体疗法,用于治疗COVID-19。预计全部订单会在今年第4季度运输完成,将带来大约3.3亿美元的收入。
2020年初,君实生物与中科院共同开发了针对新冠病毒的中和抗体埃特司韦单抗,该抗体的海外权益于同年5月授权给礼来制药。
根据协议,礼来向君实生物支付1,000万美元首付款,并在实现规定的里程碑事件后,就JS016向君实生物支付最高2.45亿美元的里程碑款,外加该产品销售净额两位数百分比的销售分成。

I 世卫组织非洲区域办事处:非洲面临4.7亿剂疫苗缺口
根据世卫组织非洲区域主任莫提的介绍,非洲大陆目前有5000多万人完成新冠疫苗接种,仅占总人口的3.6%。
截至今年年底,非洲将从“新冠肺炎疫苗实施计划”获得共4.7亿剂疫苗,使17%的非洲人口完成接种,但这个数据远远低于全球40%人口年底前完成接种的计划。非洲仍需要4.7亿剂新冠疫苗才能达成这一目标。
莫提认为,疫苗分配严重不公平的现状和交付量走低将使非洲大陆的接种率维持低位,从而导致新冠病毒变异毒株在非洲持续传播。

I Moderna总裁:德尔塔变体传染性强 “提高了新冠疫苗的标准”
Moderna总裁Stephen Hoge当地时间周三晚间表示,快速传播的德尔塔变体传染性强,它暴露了疫苗保护方面的弱点,并改变了结束疫情的前景。
他在接受电话采访时说,德尔塔变体“非常擅长感染和复制,以至于提高了疫苗质量的标准。它实际上提早暴露了(疫苗)的一些弱点。”
I 辉瑞:全美自愿召回所有批次「禁烟药Chantix」
Chantix是辉瑞的重磅戒烟药,可有效缓解对尼古丁的渴求和戒断症状,而且可以在12周的治疗中帮助减少吸烟的快感。Chantix此前被批准用于帮助吸烟者戒烟,但该药物仅用于短期治疗。

日前,辉瑞已自愿召回12批次戒烟药Chantix,召回的理由是Chantix中的致癌杂质亚硝胺含量超过规定的每日可接受摄入量(ADI)。辉瑞目前已暂停了Chantix的分销,并正在加速对Chantix进行内部测试。
辉瑞昨日(9月16日)最多走低超4%。
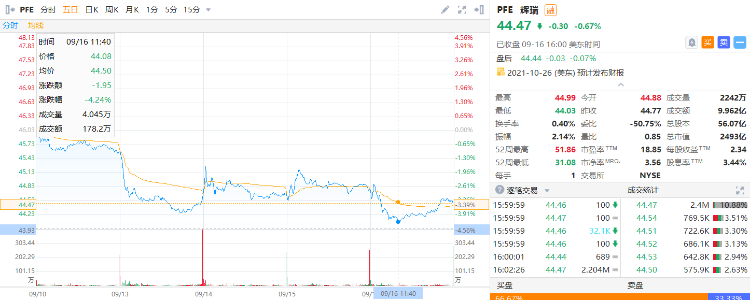
来源:华盛通
I 赛生药业:引进肿瘤药「HSP90-PI3K小分子偶联药物」大中华区独家权益
9月16日,赛生药业宣布,与Tarveda Therapeutics公司达成合作与许可协议,将作为Tarveda独家合作伙伴在大中华区(包括中国大陆、中国香港、中国澳门及中国台湾)开发、生产和商业化新型小分子偶联药物产品组合。
此次赛生药业引进的产品组合通过结合已激活的HSP90,将有效载荷泛PI3K抑制剂选择性地递送至实体瘤中,并通过连接体掩盖泛PI3K抑制剂的活性,直至其在肿瘤中获优先释放,从而进一步增强有效载荷的耐受性。
此次合作是赛生药业与Tarveda继2020年3月就小分子偶联药物PEN-866签订大中华区独家许可协议后,再一次基于Tarveda的Pentarin小分子偶联药物开发平台达成的产品开发和商业化合作。

截至发稿,赛生药业涨4.07%,报11.76港元。
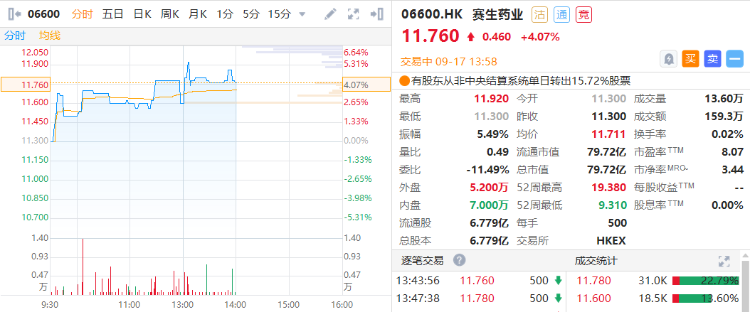
来源:华盛通
I 微创医疗建议分拆上海微创医疗机器人保证购买配额
微创医疗科学倘建议分拆上海微创医疗机器人(集团)于联交所主板独立上市得以进行,将以优先发售之方式向集团合资格股东提供全球发售项下初步提呈发售之约5%的分拆公司股份之保证配额,厘定合资格股东的保证配额之记录日期将为下个月(10月)4日,并暂停办理股份过户登记手续。买卖合资格享有保证配额股份的最后日期将为9月28日。

I 已投入 11 亿!复宏汉霖「 PD-1 一线鳞状 NSCLC 适应症」报上市
9月16日,CDE官网显示,复宏汉霖斯鲁利单抗(HLX10)注射液上市申请获受理。据推测,适应症是sqNSCLC。
复宏汉霖在2021年中期业绩报告中提到,斯鲁利单抗联合化疗一线治疗局部晚期或转移性鳞状非小细胞肺癌(sqNSCLC)的全球多中心III期临床试验已完成受试者招募入组,计划于2021年下半年就该适应症向NMPA递交NDA。

来源:CDE官网
I 「CD20/CD3双抗」获批临床,诺诚健华和康诺亚生物合作开发
9月16日,诺诚健华和康诺亚生物联合宣布,已经收到中国国家药品监督管理局(NMPA)核准签发的《药物临床试验批准通知书》,同意双方合资公司天诺健成研发的CD20 x CD3双特异性抗体CM355开展CD20+B细胞血液瘤的临床试验。
根据新闻稿,CM355可以特异性结合CD20阳性靶细胞和CD3阳性T细胞,将免疫T细胞招募至靶细胞周围,激活T细胞,诱导T细胞介导的肿瘤细胞杀伤(TDCC)作用杀伤靶细胞,用于治疗CD20+B细胞血液瘤。

来源:CDE官网
I 基石药业-B:「CS2006/NM21-1480」在中国的临床试验申请获批准
CS2006/NM21-1480是一种靶向PD-L1、4-1BB和人血清蛋白(HSA)的单价三特异性抗体。
根据其分子设计, CS2006/NM21-1480仅在与肿瘤细胞表面的免疫检查点配体PD-L1结合的情况下,才能条件性地诱导免疫共刺激受体4-1BB,激活抗癌T细胞,从而可能避免使用传统4-1BB激动剂抗体时所观察到的肝毒性。作为一种潜在同类最优疗法,CS2006/NM21-1480可用于单药治疗或与多种疗法联合治疗。
即将开展的临床试验旨在评估CS2006/NM21-1480在多种晚期实体瘤中国患者中的安全性、药代动力学特征及抗肿瘤活性。

来源:基石药业官微
风险及免责提示:以上内容仅代表作者的个人立场和观点,不代表华盛的任何立场,华盛亦无法证实上述内容的真实性、准确性和原创性。投资者在做出任何投资决定前,应结合自身情况,考虑投资产品的风险。必要时,请咨询专业投资顾问的意见。华盛不提供任何投资建议,对此亦不做任何承诺和保证。
推荐文章
一周财经日历 | 压轴登场!小米、拼多多等重磅财报来袭;深演智能、云英谷科技等新股下周上市;港美股下周一休市一日
港股周报 | 利好共振!芯片股集体狂飙,兆易创新周涨超43%;阿里致股东信:将AI+云打造成新增长动力;联想飙涨20%刷历史新高
美股机会日报 | 今晚11点!特朗普将亲自“加冕”美联储新主席沃什;英伟达Vera Rubin机架售价狂飙!产业链所有组件迎涨价热潮
SpaceX在发现多项问题后推迟“星舰”第12次试飞
华盛早报 | 沃什今晚11点宣誓就职美联储主席!雷军称未来两年内存或持续涨价;Q1恒指季检结果今晚公布
特朗普再威胁伊朗交出浓缩铀!称到手后或销毁
美股机会日报 | 伊朗称高浓缩铀不得运往国外;特朗普再出手!美国政府20亿美元布局量子计算;SpaceX正式递表冲刺纳斯达克
一图看懂 | 连续两季盈利!蔚来Q1经营利润0.66亿元,交付量超8万辆;毛利率创近四年新高

