原创精选> 正文
药闻头条丨首个国产新冠抗体药物加速生产!荣昌生物今日登陆科创板
2022-03-31 13:38
编辑:OrlyWu
I 腾盛博药与国药控股达成合作,共同商业化新冠中和抗体
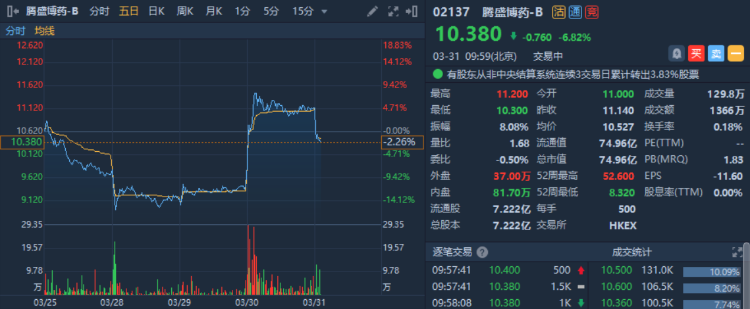
3月30日,腾盛博药宣布,其子公司腾盛华创与国药控股达成战略合作,双方将共同携手推进公司长效新冠单克隆中和抗体安巴韦单抗/罗米司韦单抗联合疗法在中国的商业化进程,包括药品储备、渠道分销、区域准入、及其它创新业务合作。
2021年12月8日,该联合疗法获得国家药监局(NMPA)批准上市,用于治疗轻型和普通型且伴有进展为重型(包括住院或死亡)高风险因素的成人和青少年(12-17岁,体重≥40 kg)新型冠状病毒感染(COVID-19)患者。
昨日腾盛博药大涨,盘中一度涨近8%,今日回落,现报10.38港元/股。
I 国务院发布《“十四五”中医药发展规划》
3月29日,国务院办公厅印发《“十四五”中医药发展规划》,这是首个以国务院办公厅名义印发的中医药五年规划。《规划》部署了十方面重点任务,包括建设优质高效中医药服务体系,提升中医药健康服务能力,建设高素质中医药人才队伍,建设高水平中医药传承保护与科技创新体系,推动中药产业高质量发展,发展中医药健康服务业,推动中医药文化繁荣发展,加快中医药开放发展,深化中医药领域改革以及强化中医药发展支撑保障,并安排了十一类共四十四项重大工程项目。

I 荣昌生物登陆科创板,挺进“A+H”时代
3月31日,荣昌生物制药(烟台)股份有限公司登陆科创板,正式挺进“A+H”时代。
2020年11月9日,荣昌生物在港交所上市,以5.9亿美元创下当年全球生物技术IPO募资最高纪录。截至发稿,荣昌生物在20多个国家或地区累计拥有85 项已授权专利(其中发明专利64项),并有超过140项在申请专利,为泰它西普、维迪西妥单抗等产品构筑起全球竞争的专利护城河。

I 美国FDA于周二正式批准为50岁以上群体使用第二剂新冠加强针
3月29日,FDA 周二批准了Pfizer/BioNTech的Comirnaty或Moderna的Spikevax的第二剂COVID-19加强剂量,用于老年人和某些免疫功能低下的个体。
这两种mRNA疫苗的紧急使用授权 (EUA) 扩大后,允许在接受过任何授权或批准的 COVID-19 疫苗的第一剂加强针后至少四个月将它们用于 50 岁及以上的个人。

来源:推特
I 2300元/盒!辉瑞新冠口服药Paxlovid于中国内地定价流出,已纳入医保
2022年3月21日,国家医保局对《新型冠状病毒肺炎诊疗方案(试行第九版)》新增的奈玛特韦片/利托那韦片,已纳入医保支付范围。
目前,辉瑞新冠口服药奈玛特韦片/利托那韦片组合包装(Paxlovid)在浙江投入使用,价格为2300元/盒。该药在美国的定价为:为期5天疗程,美国政府需要支付约530美元(约合人民币3367元)。

I 信达生物与礼来深化肿瘤领域战略合作
3月28日,信达生物在港交所公告,公司与礼来制药宣布鉴于双方致力使创新药物惠及更多中国患者的共同愿景,同时依托自身优势取得双赢,双方将深化战略合作,就以下事项达成协议:公司获得在中国大陆进口、销售、推广和分销希冉择 (雷莫西尤单抗)和 Retsevmo (塞普替尼)获批后独家商业化权利,以及授予公司享有Pirtobrutinib未来在中国大陆商业化权利的优先谈判权。

I 百健与伊奥尼斯合作渐冻症疗法临床试验失败,宣告终止
3月28日,Biogen和合作伙伴Ionis Pharmaceuticals联合公告,在研肌萎缩侧索硬化症(ALS)治疗BIIB078未能通过 I 期试验,临床计划将停止。据称,该反义寡核苷酸药物未达到该研究的任何次要疗效终点,也未证明对C9orf72相关疾病患者的临床益处。

风险及免责提示:以上内容仅代表作者的个人立场和观点,不代表华盛的任何立场,华盛亦无法证实上述内容的真实性、准确性和原创性。投资者在做出任何投资决定前,应结合自身情况,考虑投资产品的风险。必要时,请咨询专业投资顾问的意见。华盛不提供任何投资建议,对此亦不做任何承诺。
推荐文章
华盛早报 | 英特尔大涨11%,斩获谷歌芯片大单!获黄仁勋力挺,高通盘后一度涨超8%;OpenAI称已提交IPO申请
新股申购 | 无线传感SoC龙头SENASIC今起招股,一手入场费3709.04港元
6月9日外盘头条:SpaceX上市获大幅超额认购 OpenAI提交美国IPO申请 苹果WWDC26 库克谢幕 系统提速
继Anthropic之后,OpenAI也提交了美国IPO申请
高盛、摩根大通探索全新工具管控人工智能信贷风险
期权交易指南 | 美股大跌要抄底or止盈?这五张期权值得关注;太空ETF或将上演最后的疯狂
华尔街面临“三重威胁”:伊战风险、AI估值泡沫与美联储加息预期
黄仁勋抵达韩国 在首尔烤肉店与韩企众掌门共进晚餐

