原创精选> 正文
FDA年底有点忙!数十亿美元的机会,谁将从中“分羹”?
2021-10-15 19:53
- 辉瑞(PFE) 0
- 艾伯维公司(ABBV) 0
- Avadel制药(AVDL) 0
当地时间10月14日,美国食药监局FDA的外部专家顾问一致给Moderna的新冠疫苗加强针开了绿灯。这意味着,FDA可能很快批准部分美国国民接种第二种新冠疫苗的加强针。
最近几周,FDA关于Moderna疫苗加强针的决定一直是投资者关注的焦点,但该机构在未来几个月还有很多重要的事情要做。
今年年底前,FDA将宣布几项价值数十亿美元的决定,预计影响辉瑞、礼来以及Intra-Cellular Therapies等大小生物技术公司的股价。
以下是FDA年底之前要做出的重大决定:
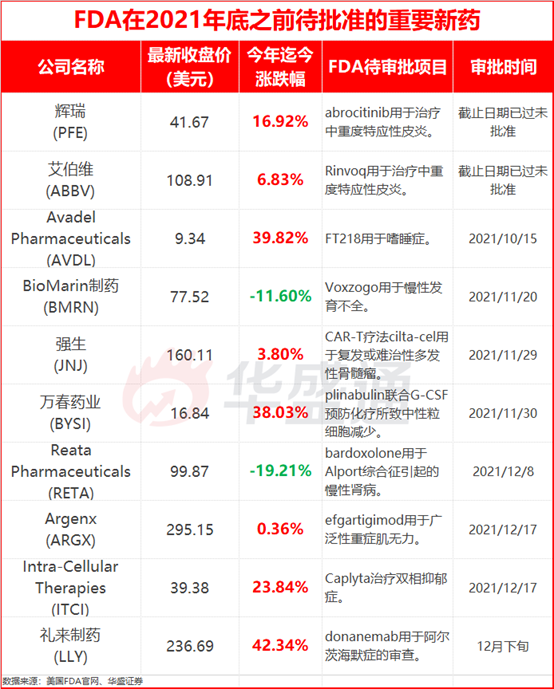
一、备受争议的阿尔茨海默症治疗药物
早些时候,尽管大众强烈反对FDA批准百健公司 $BIIB 的阿尔茨海默症治疗药物Aduhelm,但FDA仍然批准了该药。
今年年底前,礼来制药 $LLY 预计也将提交一份加速批准其阿尔茨海默症治疗药物donanemab的申请,届时,FDA需要对其进行审批。
Cantor Fitzgerald公司的分析师Louise Chen说:“考虑到围绕百健公司Aduhelm所引发的众多争议,FDA也有可能会拒绝礼来的申请,若真是这样,那对礼来来说绝对是糟糕的一天。”
礼来今年股价上涨超40%,这在很大程度上是因为FDA意外地批准了Aduhelm后,投资者对donanemab抱有很大的期待。若此次FDA礼来申请不通过,不仅礼来的股票将暴跌,可能还会拖累其他开发阿尔茨海默病药物的的公司股价,包括罗氏 $RHHBY 和百健等。
二、悬而未定的JAK抑制剂
FDA也将决定一种名为JAK抑制剂的药物类别的未来。
JAK抑制剂用于治疗类风湿性关节炎和其他炎症。FDA非常关心这类药物的安全性,今年9月,美国FDA要求修订某些JAK抑制剂说明书,增加关于严重心脏相关事件、癌症、血栓和死亡风险的黑框警告。
与此同时,辉瑞 $PFE 和艾伯维 $ABBV 都在等待FDA是否批准其JAK抑制剂治疗特应性皮炎的决定,目前辉瑞的abrocitinib和艾伯维的Rinvoq等该类型药物已经过了的最后审批期限。
现在,FDA需要决定JAK抑制剂作为关节炎治疗药物应如何应用于不同的医学领域,由FDA的不同部门监督,缺乏专员可能会使这一任务更加困难。
JAK抑制剂的批准也将使投资者了解到FDA是如何看待这一类别药物的,并将对因塞特医疗 $INCY 和礼来等拥有此类药物的公司产生影响,而不仅仅是辉瑞和艾伯维。
三、杰富瑞预计年底有望获批的公司
规模较小的公司也在等待FDA决定,因为这可能对其股价产生重大影响的。
FDA将在12月17日前决定是否批准Intra-Cellular Therapies公司 $ITCI 治疗双相抑郁症的药物Caplyta。杰富瑞(Jefferies)分析师Andrew Tsai表示,他认为该药将获得批准,而该公司的股价将从最近的39美元升至55美元。
FDA预计将在12月17日之前批准Argenx公司 $ARGX efgartigimod作为重症肌无力的治疗药物。杰富瑞(Jefferies)分析师Akash Tewari在10月初表示,他相信该公司的药物将在今年获得批准,并将该股目标价提高到362美元。
风险及免责提示:以上内容仅代表作者的个人立场和观点,不代表华盛的任何立场,华盛亦无法证实上述内容的真实性、准确性和原创性。投资者在做出任何投资决定前,应结合自身情况,考虑投资产品的风险。必要时,请咨询专业投资顾问的意见。华盛不提供任何投资建议,对此亦不做任何承诺和保证。
推荐文章
美股机会日报 | 进军光通信赛道!英特尔力争全球首个玻璃基板量产席位;特朗普再现“喊单”操作!美光盘前大涨7%
华盛早报 | 美伊或周二官重开霍尔木兹!布、美两油大跌近6%;华为韬(τ)定律引爆半导体产业链;小米今日将公布Q1财报
财报前瞻丨小米Q1财报将迎“至暗时刻”?华尔街料Q1净利降近50%,高盛、大摩仍逆势唱多!
休市提醒 | 港美股5月25日休市一日
一周财经日历 | 压轴登场!小米、拼多多等重磅财报来袭;深演智能、云英谷科技等新股下周上市;港美股下周一休市一日
港股周报 | 利好共振!芯片股集体狂飙,兆易创新周涨超43%;阿里致股东信:将AI+云打造成新增长动力;联想飙涨20%刷历史新高
美股机会日报 | 今晚11点!特朗普将亲自“加冕”美联储新主席沃什;英伟达Vera Rubin机架售价狂飙!产业链所有组件迎涨价热潮
特朗普再威胁伊朗交出浓缩铀!称到手后或销毁

