原创精选> 正文
药闻头条丨又一家药企放弃新冠疫苗研发!翰森制药4.5亿美元进军siRNA
2021-10-14 10:37
I CureVac宣布放弃新冠mRNA疫苗研发,后续开发重心转移到第二代疫苗
10 月 12 日,CureVac宣布从 EMA 批准程序中撤出其第一代COVID-19候选疫苗CVnCoV,这一决定也意味着该公司与欧盟委员会此前达成的4.05亿剂疫苗预采购协议将终止。
根据CureVac官方公告,第一代COVID-19mRNA 疫苗CVnCoV预计最早在2022年Q2才能获批。鉴于当前疫情形势的发展变化,CureVac认为有效应对病毒和新出现的变种的要求已经改变,将后续开发重心转移到与葛兰素史克合作的第二代疫苗上更有助于解决公共卫生需求。
该公司期望在 2022 年上半年将二代 mRNA 疫苗推进到后期临床,并在同年争取监管部门批准。
而在9月28日,法国制药巨头赛诺菲宣布,停止信使核糖核酸新冠疫苗的三期实验,原因在于该款疫苗已经错过投放市场的最佳时机,该公司表示将继续推进重组蛋白新冠疫苗的研发工作。

来源:公司官网公告
昨日,CureVac收涨6.61%,报43.90美元,总市值为82.09亿美元。
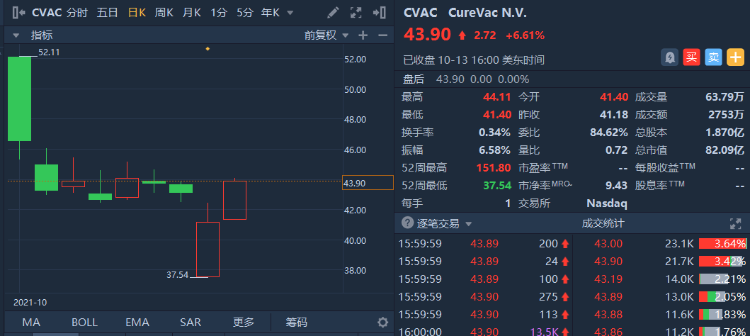
来源:华盛通
I FDA批准默沙东K药联合化疗一线治疗宫颈癌
10月13日,默沙东宣布,美国FDA批准K药帕博利珠单抗与含铂化疗联用,加或不加贝伐珠单抗,一线治疗肿瘤表达PD-L1(CPS分数≥1)的持续性、复发性或转移性宫颈癌患者。
该批准基于一项关键性3期临床试验的积极结果。结果显示,与化疗相比,帕博利珠单抗+化疗将患者死亡风险降低了36%。
默沙东表示,这是首个获批一线治疗宫颈癌患者的抗PD-1疗法。

来源:公开网络
I 针对男性,默沙东九价HPV疫苗在中国启动3期临床
中国药物临床试验登记与信息公示平台显示,默沙东(MSD)近日已在中国启动“评价九价人乳头瘤病毒疫苗在中国男性中的保护效力、免疫原性和安全性”的3期临床试验。
由默沙东公司研发的佳达修9正是一款九价人乳头瘤病毒疫苗,该疫苗已于2018年4月获得NMPA有条件上市批准,适用于16到26岁的女性,用于预防HPV引起的宫颈癌、外阴癌、阴道癌、肛门癌、生殖器疣、持续感染、癌前病变或不典型病变。
此次默沙东启动的是一项针对男性群体的3期随机、双盲,以安慰剂作为对照的临床研究,旨在评价佳达修9在20至45岁中国男性中的保护效力、免疫原性和安全性。该试验计划在中国境内入组8100人,主要终点为:HPV 6、11、16、18、31、33、45、52、58相关的外生殖器和肛门内12个月持续感染,及相关的生殖器疣、阴茎/肛周/会阴上皮内瘤变(PIN)、阴茎/肛周/会阴癌。
根据今年5月发表在《柳叶刀-感染病学》(The Lancet Infection Disease)的一项研究发现,给男性接种疫苗能有效减少相关HPV感染。

来源:Chinadrugtrials
I 超4.5亿美元!翰森制药进军siRNA领域
翰森制药集团有限公司宣布,于2021年10月11日,翰森(上海)健康科技有限公司及江苏豪森药业集团有限公司,已与OliX Pharmaceuticals, Inc. (KOSDAQ: 226950)(「OliXPharamceuticals」)订立独家许可合作协议(「许可协议」)。
根据许可协议,OliX Pharmaceuticals将利用GalNAc-asiRNA平台技术,以发现先导药物并确保针对与肝脏相关的心血管、代谢及其他疾病的靶点的候选药物开发。
翰森将拥有这些疗法在中国(包括香港、澳门及台湾)(「该地域」)的独家商业权益,OliX Pharmaceuticals将拥有该地域以外其他地区的权益。OliXPharmaceuticals将收到650万美元的首付款,以及基于重要里程碑最高为4.5亿美元的款额与特许权许可分成。

来源:公司公告
I 礼来CDK4/6抑制剂获FDA批准治疗早期乳腺癌
10月13日,礼来宣布,美国FDA已经批准Verzenio扩展适应症,联合内分泌疗法(他莫昔芬或芳香化酶抑制剂),辅助治疗激素受体阳性,人表皮生长因子受体2阴性、淋巴结阳性、高复发风险的早期乳腺癌患者。
Verzenio是一款CDK4/6抑制剂,能够阻断细胞周期的进展,导致细胞衰老和凋亡。这一批准基于一项3期临床结果。结果数据显示,Verzenio联合内分泌疗法,与内分泌疗法单药相比,将患者复发的风险降低约36%。
来源:公开网络
I 治疗脑卒中!和黄医药1类化药SHPL-49注射液获批临床
10月13日,根据CDE官网,和黄医药1类新药SHPL-49注射液获批临床(受理号:CXHL2101348),拟用于治疗急性缺血性脑卒中。
上海和黄药业有限公司由和记黄埔(中国)有限公司与上海市药材有限公司于2001年8月共同投资组建,为上海首家中药合资企业。和记黄埔集团致力于中药全球化,在国内外投资成立了多家中药合资企业,并在上海张江投资成立和记黄埔医药(上海)有限公司,专注于癌症和免疫性疾病的靶向创新药物研发。据悉,这也是上海和黄药业申报的第一个1类化药。

来源:CDE官网
I 和誉医药港股上市,专注开发创新且差异化的小分子肿瘤药物
10月13日,创新药公司和誉医药完成港股上市,目前公司有14个管线,5种处于临床阶段。
公司重点产品为成纤维细胞生长因子受体(FGFR)管线组合,涵盖多类野生型及突变型FGFR异构体。除FGFR候选药物外,和誉医药管线中还包括CSF-1R抑制剂、CXCR4拮抗剂、PD-L1抑制剂等靶向主要的肿瘤微环境免疫细胞类型的药物。
根据发行价,和誉医药市值为87.53亿港元。因台风影响以及重阳节假期,港股于昨日和今日休市,该股未有二级市场价。
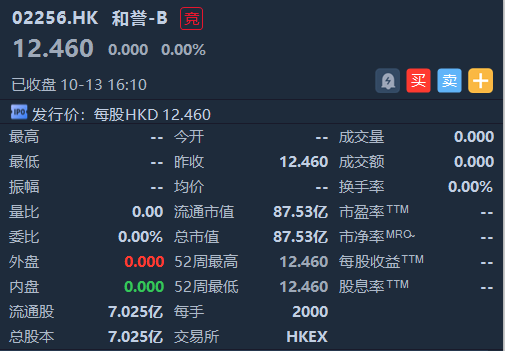
来源:华盛通
风险及免责提示:以上内容仅代表作者的个人立场和观点,不代表华盛的任何立场,华盛亦无法证实上述内容的真实性、准确性和原创性。投资者在做出任何投资决定前,应结合自身情况,考虑投资产品的风险。必要时,请咨询专业投资顾问的意见。华盛不提供任何投资建议,对此亦不做任何承诺和保证。
推荐文章
CPU重回"C位"!ARM上周暴涨超46%,还有哪些港美股标的可以上车?
美股机会日报 | 进军光通信赛道!英特尔力争全球首个玻璃基板量产席位;特朗普再现“喊单”操作!美光盘前大涨7%
华盛早报 | 美伊或周二官重开霍尔木兹!布、美两油大跌近6%;华为韬(τ)定律引爆半导体产业链;小米今日将公布Q1财报
财报前瞻丨小米Q1财报将迎“至暗时刻”?华尔街料Q1净利降近50%,高盛、大摩仍逆势唱多!
休市提醒 | 港美股5月25日休市一日
一周财经日历 | 压轴登场!小米、拼多多等重磅财报来袭;深演智能、云英谷科技等新股下周上市;港美股下周一休市一日
港股周报 | 利好共振!芯片股集体狂飙,兆易创新周涨超43%;阿里致股东信:将AI+云打造成新增长动力;联想飙涨20%刷历史新高
美股机会日报 | 今晚11点!特朗普将亲自“加冕”美联储新主席沃什;英伟达Vera Rubin机架售价狂飙!产业链所有组件迎涨价热潮

