原创精选> 正文
药闻头条 | 辉瑞:第三剂疫苗抗体暴增11倍!百济神州更新科创板招股书
2021-07-29 14:31
- 天境生物(IMAB) 0
- 辉瑞(PFE) 0
- 百时美施贵宝(BMY) 0
I 辉瑞:打第三剂疫苗,抗体暴增11倍!
辉瑞和BioNTech进行的临床试验的初步数据显示,针对受到广泛关注的Delta变种,接种第三剂疫苗后,中和抗体滴度在18-55岁成人中提高5倍以上,在65-80岁老年人中提高11倍以上。
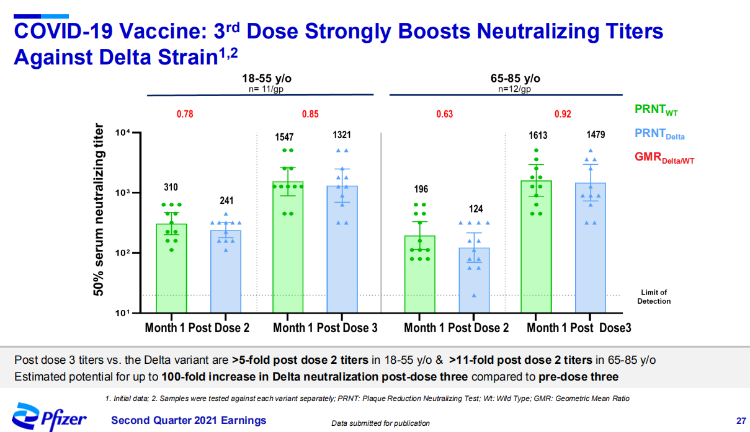
辉瑞正在与监管机构进行讨论,预计最早在今年8月递交关于追加第三剂疫苗接种的紧急使用授权(EUA)申请。同时,针对Delta变种的第一批疫苗已经完成生产,预计临床试验将在8月份开始。
I 辉瑞2021H1业绩:mRNA疫苗半年销售113亿美元
7月28日,辉瑞(PFE)公布2021年第二季度财报,上半年总收入335亿美元,同比增长68%。第二季度营收约190亿美元,扣除新冠疫苗78亿美元收入,营收达到110亿美元,同比增长10%。

从具体产品表现来看,新冠肺炎的全球大流行促使辉瑞和BioNTech合作的新冠疫苗持续放量,成为辉瑞销量最高的产品,第二季度销售收入达到78亿美元,上半年累计销售额113亿美元,预计全年将实现约335亿美元的收入。
I 百时美施贵宝:上半年营收228亿美元,Opdivo贡献36.3亿美元
7月28日,百时美施贵宝(BMS)公布2021Q2业绩,上半年总收入227.76亿美元,同比增长9%,其中Q2营收117.03亿美元,同比增长16%。
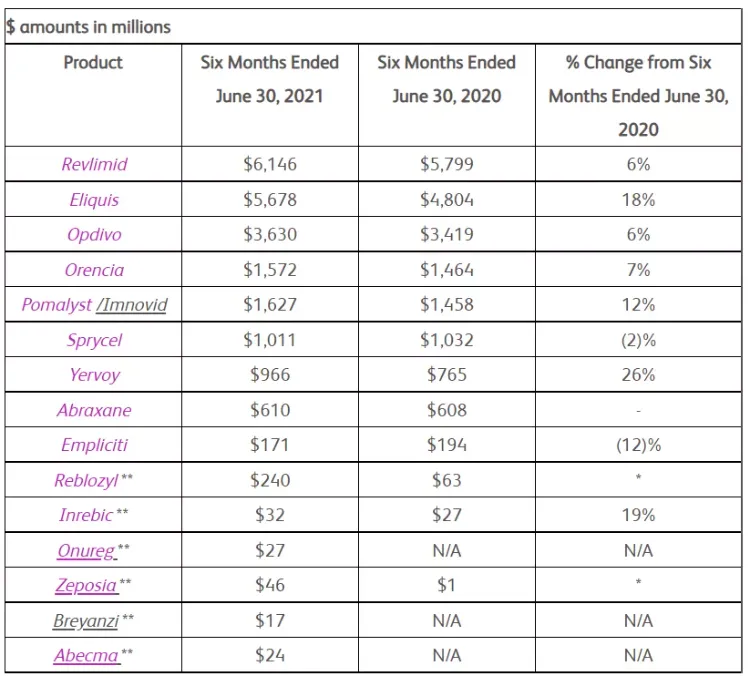
当家花旦之一Opdivo(纳武利尤单抗)上半年营收36.3亿美元,另一款免疫检查点抑制剂Yervoy也持续发力,上半年营收接近10亿美元,同比增长26%。
I 默沙东LAG-3抗体+PD-1抑制剂联合疗法临床申请获受理
7月28日,中国国家药品监督管理局药品审评中心(CDE)网站公示显示,默沙东(MSD)的1类新药MK-4280A注射液临床试验申请获得受理。公开资料显示,MK-4280A是LAG-3抗体favezelimab(MK-4280)和PD-1抑制剂Keytruda的联合治疗方案,这两款药物均由默沙东开发。

I 天境生物宣布TJ107与PD-1抗体2期联合用药临床试验申请获NMPA受理
天境生物(IMAB)7月28日宣布,中国国家药品监督管理局药品审评中心已正式受理依非白介素α(又称为TJ107/GX-I7/NT-I7)与PD-1抗体联合治疗晚期实体瘤(包括三阴乳腺癌和头颈癌)的2期临床试验申请。
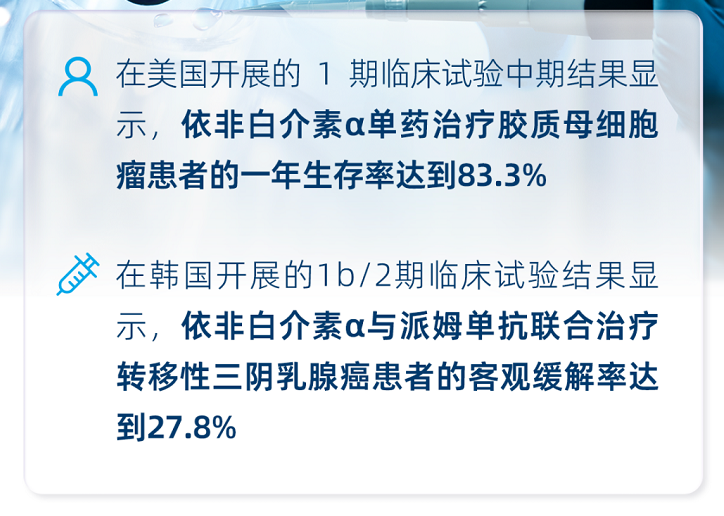
依非白介素α是全球首个也是唯一一个长效重组人白细胞介素7(rhIL-7)药物,多项临床前及临床研究显示依非白介素α通过促进T淋巴细胞增殖有效地提升T淋巴细胞数量及功能,可用于治疗肿瘤伴随性淋巴细胞减少症及联合免疫检查点抑制剂(如PD-1抗体)通过协同效应治疗肿瘤。
I 百济神州冲击A股上市:更新科创板招股书
在美国纳斯达克、港交所双重上市的中概股百济神州(BGNE.US,06160.HK)宣布,于2021年7月28日向中国证监会提交了包括更新的招股说明书在内的科创板上市注册申请材料。这也意味着,百济神州将成为第一家同时在美股、港股、A股三地上市的生物科技公司。

百济神州 ,于2016年2月8日在美国纳斯达克挂牌上市,股票代码为“BGNE”;后来于2018年8月8日,在港交所双重上市,股票代码为“06160”。
I 重磅!药品临床综合评价管理指南来袭
7月28日,国家卫生健康委办公厅印发《关于规范开展药品临床综合评价工作的通知》,对各地和各类医疗卫生机构药品临床评价工作进行部署;同时配发《药品临床综合评价管理指南(2021年版 试行)》,明确药品临床综合评价具体流程、内容与维度,聚焦技术评价与政策评价两条主线,从安全性、有效性、经济性、创新性、适宜性、可及性6个维度开展科学规范的整合分析与综合研判。
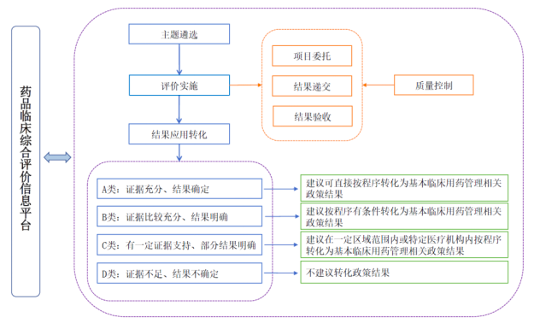
药品临床综合评价是药品供应保障决策的重要技术工具。《通知》强调,各地要以药品临床价值为导向,引导和推动相关主体规范开展药品临床综合评价,持续推动药品临床综合评价工作标准化、规范化、科学化、同质化,助力提高药事服务质量,保障临床基本用药的供应与合理使用。
风险及免责提示:以上内容仅代表作者的个人立场和观点,不代表华盛的任何立场,华盛亦无法证实上述内容的真实性、准确性和原创性。投资者在做出任何投资决定前,应结合自身情况,考虑投资产品的风险。必要时,请咨询专业投资顾问的意见。华盛不提供任何投资建议,对此亦不做任何承诺和保证。
推荐文章
一周财经日历 | 压轴登场!小米、拼多多等重磅财报来袭;深演智能、云英谷科技等新股下周上市;港美股下周一休市一日
港股周报 | 利好共振!芯片股集体狂飙,兆易创新周涨超43%;阿里致股东信:将AI+云打造成新增长动力;联想飙涨20%刷历史新高
美股机会日报 | 今晚11点!特朗普将亲自“加冕”美联储新主席沃什;英伟达Vera Rubin机架售价狂飙!产业链所有组件迎涨价热潮
SpaceX在发现多项问题后推迟“星舰”第12次试飞
华盛早报 | 沃什今晚11点宣誓就职美联储主席!雷军称未来两年内存或持续涨价;Q1恒指季检结果今晚公布
特朗普再威胁伊朗交出浓缩铀!称到手后或销毁
美股机会日报 | 伊朗称高浓缩铀不得运往国外;特朗普再出手!美国政府20亿美元布局量子计算;SpaceX正式递表冲刺纳斯达克
一图看懂 | 连续两季盈利!蔚来Q1经营利润0.66亿元,交付量超8万辆;毛利率创近四年新高

