原创精选> 正文
新股速递 | 又见细胞疗法!永泰生物也能如金斯瑞般涨十倍?
2020-03-26 10:04
作者/Oliver
国内领先的细胞免疫治疗生物医药公司——永泰生物制药有限公司于2019年9月2日第一次向港交所递交了主板上市的申请,近日,2020年3月6日,永泰生物制再次向港交所递交最新招股书申请上市。永泰生物距离香港上市更近了一步,细胞免疫治疗又一次出现在人们的视野中。
自2016年4月众所周知的魏则西事件后,中国CFDA明确将细胞免疫治疗产品划归药品管理并出台了相关管理细则。永泰生物号称是中国首家魏则西事件后拿到CFDA临床试验IND的细胞免疫治疗企业。也是中国首家完成完整临床前研究并完成申报的细胞免疫治疗企业。
在香港市场上,提起细胞治疗,那就一定得提金斯瑞生物科技,先进的CAR-T 疗法让金斯瑞走在时代的前沿,也让金斯瑞成为了十倍股,同处细胞治疗的永泰生物未来也能如此吗?
一、公司概况:肿瘤及免疫领域领先生物制药公司
永泰生物是中国最早期注册成立的专业细胞免疫治疗企业,创立于2016年11月,见证并亲身参与了中国细胞免疫治疗产业从无到有的全部过程。永泰生物聚焦细胞免疫治疗创新药领域,并已经建立了拥有细胞免疫产品研发所需要的全部技术平台,产品链覆盖了非基因修饰细胞、基因修饰细胞、肿瘤多靶点治疗细胞、肿瘤单靶点治疗细胞等全线肿瘤细胞免疫治疗产品,适应症覆盖了实体瘤和血液肿瘤,构成了阶梯性新产品梯队。

资料来源:招股书
永泰生物专注于T细胞免疫治疗药物研发和商业化,主要在研产品包括EAL产品、CAR-T细胞系列、TCR-T细胞系列等。
永泰生物的核心在研产品EAL® (扩增活化淋巴细胞)在癌症治疗的临床医用方面具有逾10年的往绩,是中国唯一获准进入实体瘤治疗II期临床试验的免疫细胞产品,为预防早期肝癌复发及延长早期肝癌患者无复发生存期及总生存期。目前EAL®产品最接近商业化,EAL®产品属多靶点肿瘤免疫细胞产品,EAL®为最初取自患者自体外周血中的T细胞经使用专利方法活化、扩增培育而成的制剂。产品以CD8+杀伤性T细 胞(表面标记为CD3分子)为主要活性成分。
二、行业概况:中国生物制剂市场前景巨大
全球癌症免疫治疗市场规模
根据弗若斯特沙利文报告,于2018年,全球癌症免疫治疗市场规模达到206亿美元。随着免疫检查点抑制剂市场的销售增长以及新治疗的批准,预计市场规模于2023年将增至755亿美元,于2030年将达到1,236亿美元。
中国细胞免疫治疗市场规模
根据弗若斯特沙利文报告,中国的细胞免疫治疗市场规模预计于2021年至2023年由人民币13亿元升至人民币102亿元,复合年增长率为181.5%。随着更多细胞免疫治疗产品获批,市场预计于2030年达人民币584亿元,2023年至2030年的复合年增长率为28.3%。
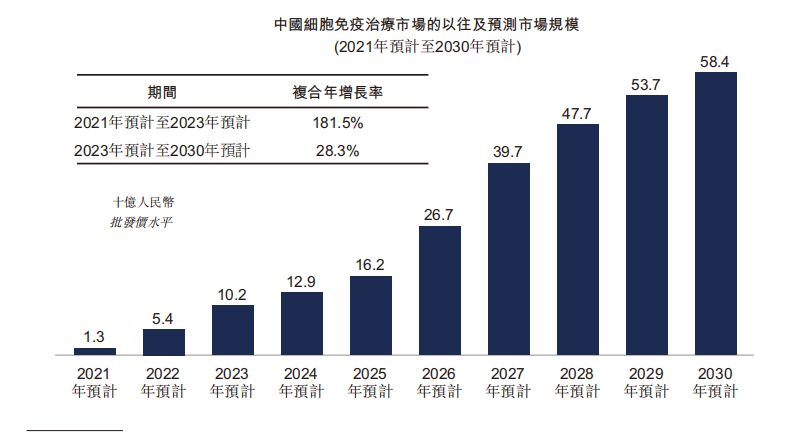
资料来源:招股书
三、财务状况
于往绩记录期间,永泰生物并无产生任何收益,而永泰生物的亏损主要来自我们的研发及行政开支。

资料来源:招股书
研发开支
截至2018年及2019年12月31日止年度,永泰生物产生的研发开支分别为人民币31.2百万元及人民币62.0百万元。随着在研产品进入临床试验,加上持续支持在研产品作为其他适应症治疗药物的临床试验,预期,永泰生物研发开支于可见将来将大幅增加。
行政开支
截至2018年及2019年12月31日止年度,永泰生物产生的行政开支分别为人民币11.7百万元及人民币27.8百万元。预计,未来行政开支将会增加,以支持业务开发工作以及(倘获批准)支持在研产品的任何商业化活动。
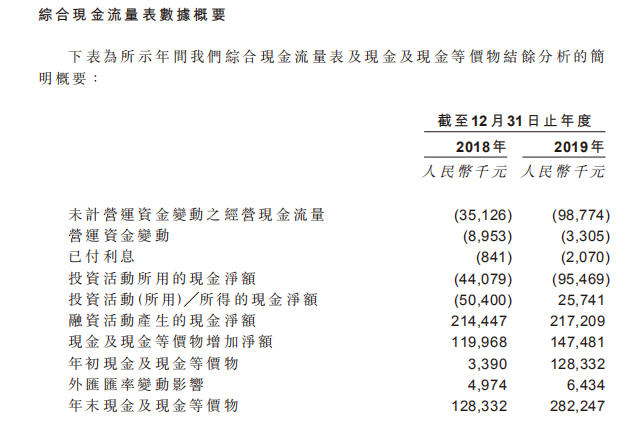
资料来源:招股书
招股书显示,截至2019年12月31日止年度,企业账面上的现金等价物约2.8亿人民币,按照董事预计,按当前公司资金消耗速度,现有资金最多能支撑公司经营和研发至2021年6月30日。
四、竞争力及风险点
竞争力方面
EAL®产品临床效果可预期,且有望在较短时间内实现商业化
EAL®产品为多靶点肿瘤免疫细胞产品,在癌症治疗的临床应用方面具有逾十年的往绩。根据永泰生物与药品评审中心进行的沟通,EAL®进行中的临床试验在中期或结束后如得到具有统计学意义的结果,则可申请批准上市。我们取得可支持EAL®产品(用于预防肝癌术后复发)有效性的临床试验结果后,可与药品评审中心就是否能够提交上市申请进行沟通交流。
在肝癌细胞治疗领域中有强劲的先发优势
永泰生物选择了肝癌术后复发作为EAL®产品临床试验的临床适应症。永泰生物相信中国肝癌临床治疗领域存在较大的市场缺口,而EAL®产品将迎来庞大的市场机遇。
高度整合的T细胞免疫治疗药物研发平台
凭借十多年来研究和应用T细胞免疫治疗技术的经验,永泰生物建立了系统性、高度整合的T细胞免疫治疗药物研发平台,包括早期研发、工艺研发、质量研究、临床前药理毒理及药物临床试验的研究平台,可以在该平台进行制度化、标准化、模块化的新产品研发,高效获得药物临床研发所需数据,快速建立产品管线。
风险点
即使获批准,永泰生物的在研产品也可能无法获得商业成功
即使获批准,永泰生物的在研产品可能无法获得来自医生、患者、第三方付款人及医学界其他各方足够的市场认可。例如,目前的化疗及放射疗法等肿瘤疗法已在医学界广为采用,而医生可能会继续倚赖该等疗法,而不考虑永泰生物的在研产品。此外,医生、患者及第三方付款人可能更青睐其他新产品,而不选择永泰生物的产品。倘在研产品并无取得合适的认可度,永泰生物可能无法产生大量的产品销售收益及可能无法盈利。
临床药物开发过程漫长、成本高昂且结果充满不确定性,而前期研究及试验的结果未必能预示未来的试验结果
不管早期结果如何,临床试验结果都可能不理想。永泰生物已经花费大量资金将相关候选药物推进到该阶段,且倘相关候选药物由于临床试验结果不佳而最终未能获得监管批准,则将不会产生任何收入。相关未补偿支出可能对我们的业务、财务状况、经营业绩及前景产生重大不利影响。
风险及免责提示:以上内容仅代表作者的个人立场和观点,不代表华盛的任何立场,华盛亦无法证实上述内容的真实性、准确性和原创性。投资者在做出任何投资决定前,应结合自身情况,考虑投资产品的风险。必要时,请咨询专业投资顾问的意见。华盛不提供任何投资建议,对此亦不做任何承诺和保证。
推荐文章
港股周报 | 科指再跌破5000点!腾讯创近一年新低!马化腾表示上了AI的船后发现“漏水了”
一周财经日历 | 英伟达、沃尔玛、百度等下周齐放榜!新主席沃什上任后首份美联储会议纪要将出炉
美股机会日报|通胀压力爆表+美拒绝伊朗停战方案,三大期指齐跌,油价一度飙涨3%;“木头姐”最新持仓出炉!再度减持特斯拉、押注太空概念
一周IPO | 中签即“吃肉”!乐动机器人、剂泰科技上市首日均涨超120%;翼菲科技孖展认购近1.49万倍,成港股新“超购王”
上市首日大涨68%!“英伟达挑战者”Cerebras创下2019年来美国科技公司最大IPO记录!(附投资分析)
华盛早报 | 特朗普持仓大曝光!大额买入英伟达、苹果;SpaceX招股说明书据悉最快下周披露!
特朗普第一季度进行3,642笔股票交易,打破数十年保密信托惯例
时隔九年再访华!特朗普携最强商业天团随行,美股半导体、存储、航空等七大板块或迎来利好

