原创精选> 正文
协同制药:下一投资佳选
2017-02-10 17:53
可以预见,美国食品药品监督管理局(FDA)批准新合力制药(NASDAQ:SGYP)的慢性特发性便秘治疗药物Plecanatide后,新合力股价会上涨,笔者已买入该股。预计2017年第一季度,新合力将提交Plecanatide的新药申请,用于治疗肠易激综合征(CIC)和肠易激综合征便秘型(IBS-C)。
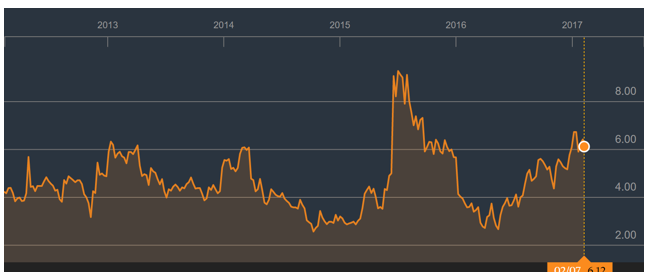
(图表来源:Bloomberg)
据新合力预测,美国330万及全球14%的人口将遭受CIC困扰。Plecanatide的目标人群CIC和IBS-C患者,仅在美国就有450万。
新合力旗下Plecanatide的临床治疗效果与其竞争对手Ironwood制药公司(NASDAQ:IRWD)的药物Linzess相当,但Plecanatide的副作用更少,发生腹泻或导致停药的几率更小。Linzess 2015年度销售额为6.25亿美元,预计至2020年,该数额将超10亿美元。
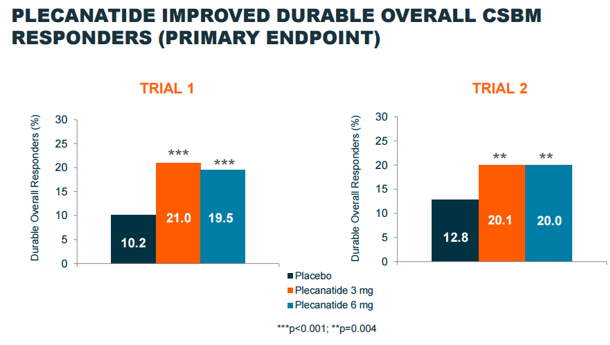
(Plecanatide在两次关键的三期试验中用于治疗CIC的临床治疗表现数据,来源:company presentation)
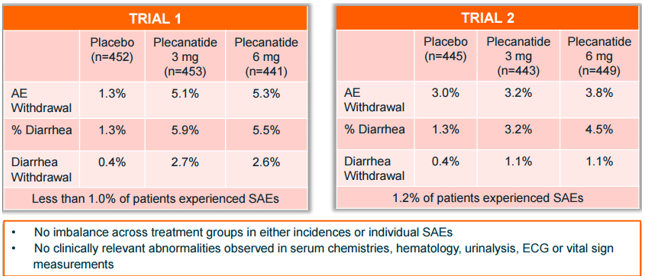
(Plecanatide在两次关键的三期试验中用于治疗CIC的安全性数据,来源:company presentation)
潜在竞争对手分析(来源:季报)
现有治疗药物:Lubiprostone,Linaclotide,Prucalopride。
研发中药物:Albireo制药(NASDAQ:ALBO)公司的Elobixibat,在日本和亚州处于三期研发阶段。
Dolcanatide,用于治疗轻度至中度溃疡性结肠炎的尿鸟苷素类似物,处于二期试验阶段。
Ironwood制药和艾尔建(NYSE:AGN)近日宣布FDA批准可将较低剂量(每日72微克)的Linzess用于CIC治疗,并提到在之前的三期试验第二阶段中,较低剂量的药物也能达到预期治疗目标,这在统计学上意义重大。此外,用量减少后,药物造成的腹泻及由腹泻导致的停药率降低。通过查阅医学文献及该公司的SEC备案文件,笔者并未发现Linzess临床效用的具体数据,如缓解率,也未发现不良反应相关的详细信息,如药物可能引起的腹泻或腹泻导致停药的发生率。每日服用3毫克Plecanatide的缓解率与每日服用145毫克Linzess缓解率相当,因此笔者预计每日服用72微克Linzess对于病情的缓解率会低于每日服用3毫克Plecanatide的缓解率。因此笔者仍更看好新合力制药。
IBS-C:2016年末三期试验第一阶段成功。每日服用3毫克和6毫克的总缓解率分别为21.5%和24%。最常见不良反应为腹泻,其中每日服用3毫克和每日服用6毫克的腹泻率分别为3.2%和3.7%。
财务状况与股票估值:
新合力制药近期通过以每股6.15美元的价格二次发行203.2万股股票募资。公司目前现金储备达2050万美元,长期负债为761万美元。预计其现金支出为每季度3000万美元左右。
Plecanatide患者每年使用该药物所需费用为4500美元,与每日服用145毫克Linzess的价格相当,美国有330万CIC患者,通过模拟计算,截至2026年Plecanatide专利到期,新合力在美国的销售额最高可达17.2亿美元。而Linaclotide截至2020年的最高销售额为10至20亿美元。
根据企业现金流贴现模型(DCF),即前5年的贴现率为15%,然后是12%,最低为10%,笔者通过计算得出未来风险调整后的营收净现值为256万美元。用调整后的非营业资产(包括最近的股票发行)和负债,以稀释后的股本计算,协同制药的每股公允价格为11.5美元,这也是笔者的第一价格目标。此外,该公司目前的股价十分吸引人,武田制药(OTCPK:TKPHF),艾尔建等公司都对其有收购意向。
文章来源:seekingalpha
免责声明:本文仅供参考,并非投资建议,我们将竭力提供专业可靠的信息。转载请注明来源,本公司将保留所有法律权益。
推荐文章
提价83%需求却暴增400%!智谱、MiniMax锁定大模型定价权,AI Agent元年即将开启?
港股见底了吗?北水大举加仓逾600亿港元!大行看好4月做多窗口来临,十大金股一图睇全
华盛早报 | 伊朗与阿曼拟共管霍尔木兹!美股V型反转;伊朗袭击甲骨文、亚马逊数据中心;港美股今日因假期休市一天
诺和诺德称:口服版Wegovy减肥效果优于礼来GLP‑1口服药
美股机会日报 | 特朗普粉碎停战幻想!恐慌指数飙升12%,纳指期货跌约2%;美油期货暴涨超9%!油气股飙升,美国原油基金ETF涨超9%
清明休市提醒 | 港股本周五休市,下周三恢复交易;美股周五休市一天
油价上涨 此前特朗普表示伊朗冲突可能在未来几周升级
野村:特朗普讲话未能发出局势降温的明确信号

