熱門資訊> 正文
從「中國落地「到「全球創新「:遠大醫藥(00512)核藥收入激增106%背后的創新生態
2025-08-20 08:47
- 遠大醫藥(00512.HK) 0
- 歐文斯科寧(OC) 0
- 羅文(RDC) 0
今年以來,遠大醫藥(00512)連續取得多項重磅創新進展,創新研發成果豐碩。近日,公司公佈2025中期業績,進一步彰顯其高質量發展態勢。2025年上半年,遠大醫藥營收再創新高,取得約61.1億港元(其中創新壁壘產品收入佔比約51%);淨利潤約11.7億港元。業績的穩健增長與公司保持高強度研發投入密切相關,上半年,遠大醫藥研發投入約10.2億港元,推動新增38項重大研發里程碑,其中創新產品16項。
穩健增長的業績背后,是公司堅持科技創新、產品連破紀錄、產能全球領跑的「三連擊」——6月底,《支持創新葯高質量發展的若干措施》出臺;7月1日,醫保局迅速落地目錄調整方案並首次明確「新葯首發價格機制」,為創新葯掛網、定價劃出「穩定期」,進一步為遠大醫藥創新增長賦能。
政策東風正勁之際,遠大醫藥的里程碑密集落地:易甘泰®釔[90Y]微球注射液以98.5%客觀緩解率提前獲FDA批准新增原發性肝癌適應症,成為全球唯一同時覆蓋肝癌與結直腸癌肝轉移的內放射治療產品;此外,在2025年商保初審目錄中,公司釔[90Y]、OC01等多款創新產品被成功被納入;前列腺癌治療RDC藥物TLX591獲批加入國際多中心Ⅲ期臨牀;成都温江全球首個「零輻射」智能核藥工廠正式投產。
這些里程碑,正是遠大醫藥「Go Global」戰略的生動註腳:憑藉覆蓋歐美日的成熟臨牀與商業化網絡,公司自主操盤國際多中心試驗,靈活嫁接全球渠道,迅速放大產品滲透率。尤其在覈藥賽道,依託世界領先的全產業鏈優勢,遠大醫藥正獨立推進海外研發、註冊與銷售,全面提升在全球競爭中的主動權和話語權,讓中國核藥真正走向世界,讓創新成果更早惠及全球患者。
納入商保目錄+獲FDA新適應症,釔[90Y]生長勢頭正茂
作為全球僅有的四家實現創新核藥商業化的藥企之一,遠大醫藥核藥板塊已率先步入收穫期,併成為公司業績爆發的核心引擎。
2025年中報顯示,遠大醫藥核藥抗腫瘤診療板塊收入錄得約4.2億港元,再次實現超100%的大幅增長。
易甘泰®釔[Y90]微球注射液是遠大醫藥核素藥板塊的核心產品,在2002年5月獲得美國FDA批准上市,並於2022年1月獲得我國藥監局的上市許可,主要應用於肝癌的選擇性內放射治療(SIRT),用於治療不可手術切除結直腸癌肝轉移、中晚期原發性肝癌等。
根據GLOBOCAN 2022年的數據,全球新發肝癌87萬例(第6位),死亡76萬例(第3位)。中國2022年新發37萬(佔全球42.5%,全國第4位),死亡32萬(佔全球42.1%,全國第2位),病例及死亡均居全球首位。
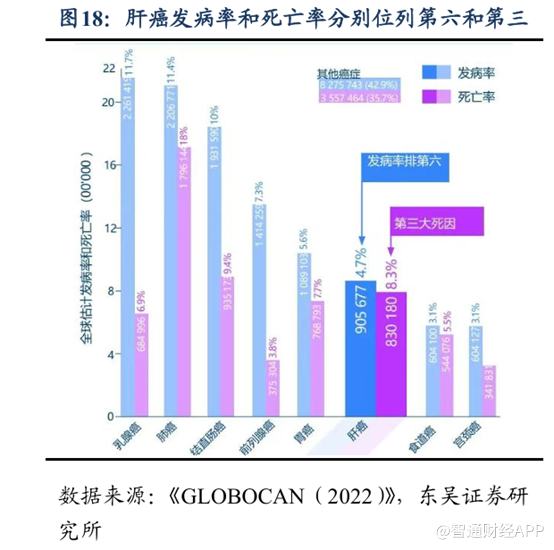
目前,手術切除是治療早期HCC的首選方法,但由於肝癌發病隱匿,早期症狀不明顯或不典型,早期確診困難,不足30%的肝癌患者在初診時適合根治性治療,但治療棘手,因此預后較差,發病率與死亡率之比高達1:(0.8~0.9);即使通過根治性切除,肝癌切除術后5年腫瘤復發轉移率也高達50%~70%;在北美地區的5年生存率不到20%,而在中國更低,僅有12%。根據Grand View Research, Inc.報告,2030年全球肝癌治療藥物市場規模預計將達到98.1億美元。
從現有的肝癌治療格局來看,臨牀仍期待更為有效的治療方式。釔[90Y]微球注射液是一款針對肝臟惡性腫瘤的選擇性內放射治療(SIRT)產品,採用介入技術將釔[90Y]樹脂微球注入肝臟腫瘤血管,釋放高能量β放射線殺滅腫瘤細胞。
海外臨牀中期數顯示,釔[90Y]用於治療不可切除HCC的客觀緩解率高達98.5%;所有可評估患者均顯示治療反應,提示局部腫瘤控制率達到100%;此外,中位緩解持續時間超過300天。
基於上述突破性中期臨牀數據,FDA提前正式批准了該產品用於不可切除HCC的適應症,且未限制腫瘤直徑大小。值得注意的是,波士頓科學的釔[90Y]玻璃微球治療HCC對於腫瘤直徑存在1-8cm的限制,遠大醫藥釔[90Y]微球注射液治療HCC無腫瘤直徑大小限制獲批這一突破性進展也反映了其顯著的產品優勢及臨牀價值。
今年以來,釔[90Y]更有十余篇重磅研究成果入選2025年美國臨牀腫瘤學會年會(ASCO)及2025年亞太原發性肝癌專家會議(APPLE 2025)等國際權威會議,不僅展現了該產品臨牀療效的顯著優勢,更是遠大醫藥創新研發成果走向全球的實力印證。
釔[90Y]微球注射液獲批,為國內廣大肝癌患者帶來了全新且有效的治療方式。在中國上市后,釔[90Y]銷售收入的持續翻倍,進一步印證了其市場潛力。近期被納入商保初審目錄疊加后續FDA批准肝癌新適應症,釔[90Y]的生長勢頭正茂。
核藥板塊:全產業鏈佈局構築競爭壁壘
放射性核素偶聯藥物(RDC)作為一種創新的靶向治療手段,其市場正處於高速擴容期。2021年以來,全球累計達成超80項核藥交易,涉及諾華、默克、賽諾菲、阿斯利康、拜耳、強生、BMS等頭部MNC。全球前三名業務發展交易金額分別達約20.6億美元、16.3億美元及4.87億美元。
值得注意的是,諾華Pluvicto在上市僅第3年全球銷售額便超過10億美金,並在今年上半年實現約8.25億美元的收入,展示出RDC用於腫瘤治療用途的巨大潛力。
我國診療一體化核素及放射性藥物仍遠落后於歐美發達國家,絕大多數醫用放射性核素依賴進口,放射性藥物創新能力較弱,獲批上市品種極少,核醫學診療一體化臨牀應用多處於起步階段。遠大醫藥作為國內核藥領域龍頭型企業,憑藉前瞻性的精準佈局,已經率先實現了核醫學診療一體化的全產業鏈構建。
面對這百億人民幣的藍海市場,遠大醫藥圍繞腫瘤診療一體化的治療理念,在研發註冊階段共儲備了15款創新產品,涵蓋68Ga、177Lu、131I、90Y、89Zr在內的5种放射性核素,覆蓋了肝癌、前列腺癌、腎癌、腦癌等在內的7個癌種,其中4款進入III期臨牀,TLX591-CDx(前列腺癌診斷)、TLX591(前列腺癌治療)、ITM-11(胃腸胰腺神經內分泌瘤治療)、TLX250-CDx(腎透明細胞癌診斷),為患者提供多適應症治療選擇、多手段且診療一體化的全球領先的抗腫瘤方案。
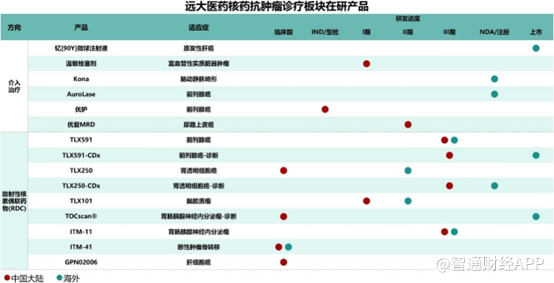
針對前列腺癌治療,遠大醫藥的TLX591已經進入到III期臨牀階段,全球進度領先。憑藉其精準靶向特性和差異化藥理學優勢,TLX591已展現出超越現有抗PSMA小肽靶向放射性配體治療(RLT)分子的臨牀潛力。TLX591僅需間隔約14天的雙劑給藥方案,相比Pluvicto等傳統PSMA RLT治療長達6周期、持續30周大幅縮短治療周期,有望重新定義PSMA陽性的轉移性去勢抵抗性前列腺癌(mCRPC)的治療標準。參考諾華的Pluvicto銷售數據,遠大醫藥的TLX591銷售收入亦有望邁入10億美金大關。
前列腺癌診斷方面,遠大醫藥的TLX591-CDx目前已在美國、澳洲、加拿大、法國等多個國家和地區獲批上市,並計劃於年內提交國內上市申請。TLX591-CDx中的靶向劑 PSMA-11 能以高親和力的方式特異性結合在前列腺癌中高表達的PSMA上,具有可內化入細胞、生物學活性穩定、體內循環半衰期短以及對腫瘤實質的滲透性好且可被非靶向組織快速清除的五大特點。
參考美國目前PSMA-PET市場,2024年 Pylarify銷售10.6億美元,luccix銷售5.2億美元。在非頭對頭的臨牀比較上,TLX591-CDx相比 Pylarify對前列腺癌復發檢測更加準確。
加上國內PSMA-PET市場競爭相對寬裕,遠大醫藥憑藉TLX591和TLX591-CDx實現前列腺癌「診療一體化」,不僅有望為中國前列腺疾病患者帶來更為精準、高效的診療方案,其搭配銷售亦能獲得更高的市場份額。
此外,遠大醫藥全球創新、基於放射性核素-抗體偶聯技術的靶向磷脂酰肌醇蛋白聚糖3 (GPC-3)的診斷型放射性藥物GPN02006早前在中國開展的研究者發起的臨牀研究(IIT臨牀研究)也取得了里程碑式突破,並在2025年北美核醫學與分子影像學會(SNMMI)年會斬獲口頭報告。
根據臨牀研究數據,GPN02006展現出卓越的安全性和顯像效能:所有受試者給藥后均未報告任何藥物相關不良反應,安全耐受性表現優異;給藥后30分鍾即可實現高質量顯像,充分滿足肝細胞癌臨牀快速診斷需求。GPN02006產品極具潛力,有望成為全球首個針對GPC-3靶點的HCC診斷類RDC產品。
遠大醫藥在覈藥賽道的連續突破,正是公司前瞻性精準戰略佈局的兑現。與此同時,公司在覈藥產業鏈方面也已形成了全方位佈局的顯著優勢。
前文提到,目前國內絕大多數醫用放射性核素依賴進口。經過多年深耕,遠大醫藥在覈藥領域已建立了完整的產業鏈,實現研發、生產、銷售、監管資質等多個環節的全方位佈局,公司產業鏈的整體佈局不僅為其核藥產業高速發展打下了堅實基礎,未來也將助力我國核素產業擺脫卡脖子問題。
今年上半年,遠大醫藥在成都温江投資逾30億元(佔地50畝)的核藥產研基地已取得甲級輻安證,標誌着公司成功搭建起覆蓋「研發-生產-銷售」全產業鏈的閉環體系,不僅打通了核藥全球化佈局的關鍵環節,更實現了從實驗室研發到工業化量產的戰略性跨越。

作為全球首個「零輻射」智能核藥工廠,該基地配備14條高標準GMP生產線,覆蓋同位素製備(如18F、64Cu、89Zr)、核藥偶聯、自動化標記等全流程。其核心突破在於以核電級安全標準構建「零輻射」智能工廠:全流程輻射監測系統,以及國際最高標準放射性操作熱室可將操作環境輻射劑量率穩定在0.2μSv/h(接近環境本底水平);通過全自動分裝系統(每分鍾處理100瓶)和中央智能控制平臺全鏈路互聯體系,使生產效率較傳統工藝提升300%,核素衰變損耗成本降低50%以上,徹底推動行業從「勞動密集型」向「智能無人化」躍遷。
更重要的是,該基地將與遠大醫藥美國波士頓研發中心、遠大醫藥-山東大學放射藥物研究院深度協同,整合全球創新資源、頂尖人才與智能製造技術,共同構成強大的全球研發與生產中心網絡。這一體系的完善,將為遠大醫藥持續加速創新核藥管線落地、打造重磅核藥品種提供堅實基礎,從而不斷鞏固其在全球核藥領域的領軍地位。
製藥科技領域多款新品密集落地,新的增長矩陣已形成
除了核藥近期頻傳利好外,遠大醫藥的製藥科技板塊也取得了多項重磅進展,包括多款新品密集落地,形成新的增長矩陣,持續夯實公司高質量發展韌性。
在呼吸及危重症領域,遠大醫藥在售產品核心產品切諾(桉檸蒎腸溶膠囊)、恩卓潤®和恩明潤®均為全國獨家品種,處於細分領域的領先地位。
恩卓潤®與恩明潤®兩款用於治療哮喘的全球創新複方製劑2022年在中國上市並進入醫保目錄,均具備「可視可控、精準吸入、一天一次」等特點,可顯著改善患者肺功能並減少急性發作風險。其中,恩卓潤®III 期臨牀研究顯示其24周中度急性發作風險的年化發生率降低了 43%;恩明潤®III 期臨牀研究顯示其針對重度、中重度和所有急性發作類別風險分別降低約 26%、22%和 19%。
產品組合可廣泛覆蓋長期哮喘治療人羣,為中國長期接受哮喘治療的人羣提供新的治療方案,提高公司在呼吸疾病治療市場的產品覆蓋,進一步夯實該領域的競爭優勢。
此外,遠大醫藥在過敏性鼻炎適應症方向也擁有多款高潛力產品佈局。目前我國成人過敏性鼻炎患病率約17.6%,患病羣體已近2.5億人口;然而診斷率僅37.3%,治療率為45.0%,存在極大的臨牀未滿足需求。根據米內網2023年數據,我國鼻用藥物市場規模近35億元,2019-2023年CAGR達10.4%,其中,布地奈德和丙酸氟替卡松的銷售基本以外資為主。遠大醫藥首仿的布地奈德鼻噴霧劑自上市以來放量顯著,未來有望進一步打破原研產品的市場壟斷。
在研品種方面,用於治療成人和兒童過敏性鼻炎的全球創新葯 Ryaltris®複方鼻噴劑已於 2024年2月在中國遞交了新葯上市申請並獲得藥監局的受理,糠酸莫米松鼻噴霧劑的註冊工作也在積極推進中。
此外,用於治療膿毒症的STC3141在今年亦取得了突破性臨牀進展,有望成為改寫全球膿毒症治療格局的重磅產品。
膿毒症是因感染引發的機體反應失調,導致急性器官功能障礙的危及生命綜合徵,已成為全球重要的公共健康負擔。根據世界衞生組織,全球範圍內每年新發膿毒症約4900萬例,超1/5的患者死亡,約佔全球總死亡人數的20%;國內重症監護病房的膿毒症發生率為20.6%~50.8%,按推測中國每年約有480萬人患有膿毒症,約1/3的患者發生院內死亡。在高收入國家,膿毒症患者的全院平均治療費用超過3.2萬美元。根據貝哲斯諮詢,2022年中國膿毒症治療市場規模約為230.7億元人民幣;根據Wise Guy Reports,2024年全球膿毒症治療藥物市場規模為125.4億美元,預計到2032年市場規模將達到193.7億美元,期間CAGR為5.58%。
STC3141是遠大醫藥自主開發的、擁有全球知識產權的、具有全新作用機制的小分子化合物,通過中和胞外遊離組蛋白和中性粒細胞誘捕網來逆轉機體過度免疫反應造成的器官損傷,可用於多種重症適應症。2025年5月,STC3141用於治療膿毒症的II期臨牀研究成功達到臨牀終點。結果顯示治療組第7天SOFA評分較基線均有明顯下降,尤其是高劑量組,降幅明顯大於安慰劑組,差異具有統計學顯著性和臨牀意義。
據智通財經APP瞭解,遠大醫藥針對STC3141採取了全球臨牀開發的策略,該產品目前已在中國、澳大利亞、比利時、英國、波蘭三大洲五個國家獲批七個臨牀批件,完成了四項針對患者的臨牀研究並全部成功達到了臨牀終點。
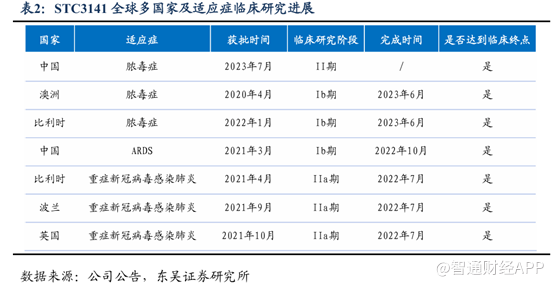
作為全球首個以重新構建免疫穩態為核心的膿毒症治療方案,STC3141針對機體免疫失調的核心病因,有望打破膿毒症領域長期缺乏針對性藥物的困境,促進全球膿毒症治療進入新紀元。
同樣的,在五官科領域,遠大醫藥針對眼科術后抗炎鎮痛、翼狀胬肉、乾眼症、近視、蠕形蟎瞼緣炎及蠕形蟎導致的瞼板腺功能障礙等存在明確臨牀需求的方向上佈局的多款創新眼藥產品也已形成良好的產品梯隊,未來商業化潛力十分可觀。

其中,全球首款治療乾眼症新葯,酒石酸伐尼克蘭鼻噴霧劑OC-01已在北京、上海、廣州等15個城市開出首批處方。作為國內首個獲批通過鼻腔給藥修復淚腺功能的創新葯,該藥的上市為乾眼開闢了「鼻內給藥」的治療新路徑。
臨牀研究顯示, OC-01產品起效迅速,可瞬時促進淚液分泌,顯著改善了乾眼症患者的原生淚液分泌量,修復淚腺功能,源頭治療乾眼。同時,一天僅需兩次鼻噴給藥,全天潤眼不傷眼,可避免傳統滴眼藥使用的繁瑣性,有望提高患者的依從性,為乾眼症患者提供一種全新的安全、有效且方便的治療選擇。
《國人乾眼多中心大數據報告》指出,中國乾眼症患者約有3.6億人;根據藥渡數據庫,預計2030年中國乾眼症藥物市場規模將增至67億美元。憑藉突出的臨牀數據,遠大醫藥的OC-01有望在龐大的乾眼市場獲取領先的市場份額。
此外,用於治療蠕形蟎瞼緣炎的全球創新眼藥GPN01768 (TP-03)海外銷售數據也十分引人注目,該產品今年上半年海外收入超1億美元,同比增長近152%。目前該產品已在中國澳門獲批上市,未來商業化潛力巨大。
隨着製藥科技板塊主力品種集採風險逐步出清,遠大醫藥正通過核藥、呼吸及危重症、創新眼藥等創新產品集羣實現極具韌性的高質量發展動能——核藥產品持續領跑,全球首創膿毒症療法STC3141與差異化眼科產品組合,依託未被滿足的臨牀需求,構築第二增長曲線。
結語
國家醫保局《若干措施》的16條新政,本質是打通創新葯「研發-支付-應用」的全生命周期閉環。憑藉核藥診療全球領軍地位、呼吸重症領域顛覆性突破、創新眼藥差異化管線三大引擎,遠大醫藥正成為政策紅利的首要承接者。
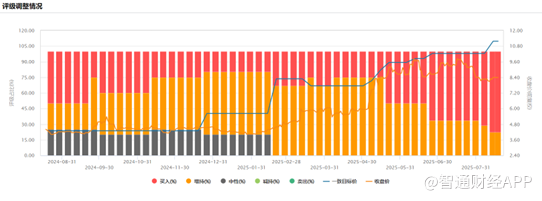
伴隨着創新引擎的強勁驅動與管線的實質性落地,遠大醫藥的戰略價值獲得資本市場高度認可,中信證券、中金公司、天風證券、西部證券、華泰金控、東吳證券等多家機構年內持續上調評級並給予「買入」,目標價從6個月前的5.62港元躍升至11.17港元(漲幅近98.8%),其中天風證券及中信證券均給出了13港元的目標價,充分印證了公司創新轉型成果與未來增長預期。
推薦文章
美股機會日報 | 凌晨3點!美聯儲將公佈1月貨幣政策會議紀要,納指期貨漲近0.5%;13F大曝光!巴菲特連續三季減持蘋果
美股機會日報 | 阿里發佈千問3.5!性能媲美Gemini 3;馬斯克稱Cybercab將於4月開始生產
港股周報 | 中國大模型「春節檔」打響!智譜周漲超138%;鉅虧超230億!美團周內重挫超10%
一周財經日曆 | 港美股迎「春節+總統日」雙假期!萬億零售巨頭沃爾瑪將發財報
從軟件到房地產,美國多板塊陷入AI恐慌拋售潮
Meta計劃為智能眼鏡添加人臉識別技術
危機四伏,市場卻似乎毫不在意
財報前瞻 | 英偉達Q4財報放榜在即!高盛、瑞銀預計將大超預期,兩大關鍵催化將帶來意外驚喜?

