熱門資訊> 正文
新股前瞻|從仿製到創新:海西新葯如何平衡現金流與研發投入?
2025-08-12 07:28
隨着華昊中天、派格生物、康樂衞士、美中嘉和等企業遞表港交所,藥企前往港股上市的熱潮還在繼續。
據港交所8月6日披露,福建海西新葯創制股份有限公司(以下簡稱:海西新葯)再次遞表港交所主板,華泰國際和招銀國際為其聯席保薦人。根據智通財經APP瞭解,該公司曾於1月3日向港交所遞表。
據瞭解,海西新葯已經進入商業化階段,憑藉多元化的產品組合及管線,實現了不小的增長。相比諸多處於臨牀階段的藥企,海西新葯發展向好性無疑是更加明顯的。
5個月營收約2.5億元最大客户貢獻營收「半邊天」
據招股書,海西新葯是一家處於商業化階段的製藥公司,集研發、生產及銷售能力於一體,具備在研創新葯的管線。公司在中國最大、增長最快的治療領域擁有多元化的產品組合及管線,目前已就14款仿製藥獲得國家藥監局批准,並建立擁有四款在研創新葯的管線,成為中國製藥行業的主要市場參與者。
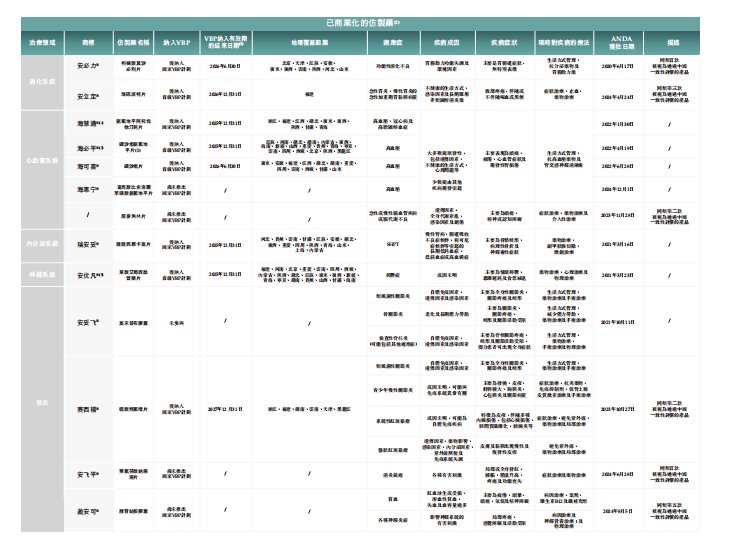
根據智通財經APP瞭解,海西新葯的發展路徑是,仿製藥和創新葯雙線佈局,在仿製藥方面,重點佈局首仿藥、難仿藥、高仿藥的研發,如MAH制度、仿製藥一致性評價以及國家藥品集採等,截至2025年7月8日,公司已商業化的產品組合主要包括用於消化系統疾病、心血管系統疾病、內分泌系統疾病、神經系統疾病及炎症疾病的仿製藥;根據灼識諮詢的資料,該等治療領域佔2023年中國醫藥銷售總額的25%以上。
在創新葯方面,海西新葯以臨牀價值為導向,專注於開發具有全球市場潛力、臨牀需求明確的小分子創新葯,包括一款潛在屬同類首款的在研腫瘤藥物、一款潛在用於治療wAMD/DME/RVO的首款口服藥物及另外兩款處於臨牀前階段,用於治療腫瘤及呼吸系統疾病的創新在研藥物。
至最后實際可行日期,公司的銷售及分銷網絡已與超過18000家醫院及其他醫療機構(包括超過5100家三級或二級醫院以及超過22000家藥店)建立聯繫,覆蓋中國所有省份、直轄市及自治區。
值得一提的是,海西新葯的經營模式也是偏輕資產的,其以藥品上市許可持有人(MAH)為核心架構。在MAH制度下,藥品上市許可與生產許可實現分離,製藥企業可將研發生產環節外包出去,這也為CMO行業帶來了新需求。
目前,海西新葯就是典型的委託CMO生產的藥企,外包模式促進了降本增效,更進一步釋放了企業盈利空間。
2022年、2023年、2024年及截至2025年5月31日止五個月(以下簡稱:報告期內),公司的分別約為2.12億元(單位:人民幣,下同)、3.17億元、4.67億元、2.49億元;同時,期內利潤分別約為0.69億元、1.17億元、1.36億元、0.9億元。業績總體呈現增長態勢。
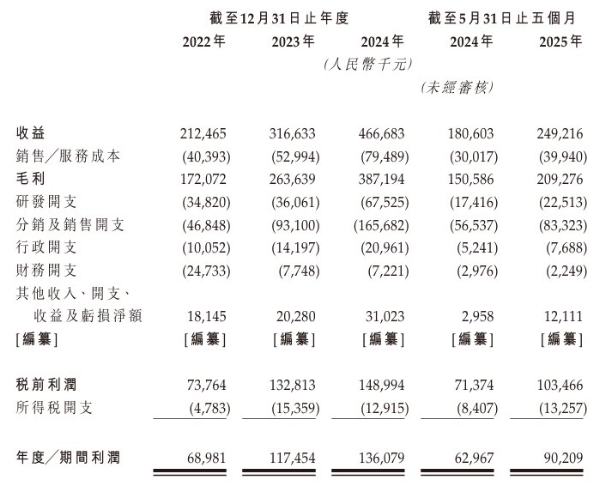
分產品而言,公司的營收主要來自於在國內銷售安必力®、瑞安妥®及海慧通®。期間,銷售該等產品的收益佔總收益分別為98.2%、92.9%、82.6%。此外,海西新葯非常依賴大客户。
期內,來自前五大客户的收益合共分別為1.81億元、2.32億元、3.39億元及1.79億元,分別佔公司總收益的85.1%、73.3%、 72.6%及71.7%。同期最大客户的收益分別為1.25億元、1.54億元、2.13億元及1.11億元,分別佔同期總收益的58.8%、48.5%、45.6%及44.5%。單一大客户貢獻營收半壁江山,對於海西新葯而言,或許並非是一件好事。
海西新葯在風險提示中坦言,由於中國獨特的VBP計劃名錄藥物採購制度,公司面臨客户依賴。倘公司的產品被剔出該等名錄或其他國家、省級或其他政府資助醫保計劃,公司與主要客户的合作將被終止,其業務、運營業績及財務狀況可能會受到不利影響。
報告期內,公司現金及現金等價物分別為1.71億元、2.54億元、3.83億元及4652.9萬元,現金流略顯緊張。
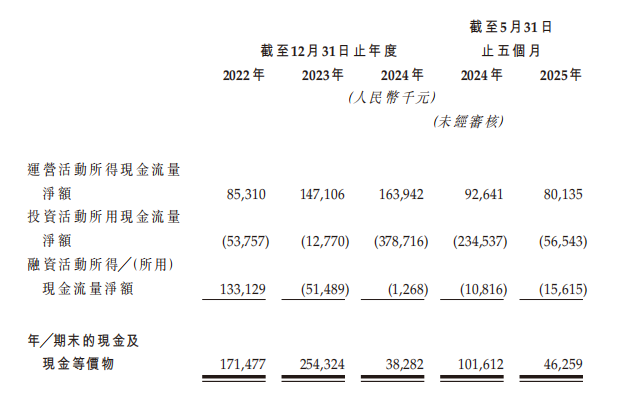
綜合來看,海西新葯依靠多元的產品矩陣、範圍較廣的渠道佈局以及輕資產架構,已經逐步打通商業化脈絡。不過,當前為海西新葯貢獻增量的基本是仿製藥。衆所周知,這一市場競爭頗為激烈,也驅使了海西新葯向創新葯市場邁進。
向創新葯市場進軍
衞健委數據顯示,目前4000多家中國製藥企業中,90%以上都是仿製藥企業;全國17萬藥品批文中,95%以上都是仿製藥。需要注意的是,以「仿製」為主的產品開發路徑,也意味着相關藥企的護城河並不堅固,參與市場競爭難以具備絕對優勢。
基於對上述問題的洞察,以及創新葯相關政策的激勵,近年海西新葯愈發重視「創新」二字。
據悉,海西新葯的創新葯管線包括1個2期臨牀項目、3個臨牀前項目,覆蓋了腫瘤、眼科及呼吸系統疾病領域需求。
其中截至最后實際可行日期,公司已(i)啟動C019199用於骨肉瘤及TGCT的Ib/II期臨牀試驗;(ii)啟動C019199結合抗PD-1單克隆抗體用於治療三陰性乳腺癌(TNBC)、結直腸癌及胰腺癌的聯合療法II期臨牀試驗。於2025年,公司預計將完成HER2陰性乳腺癌單藥治療的II期臨牀試驗。於2026年上半年,公司預計將在中國啟動C019199結合抗PD-1單克隆抗體聯合治療骨肉瘤及TNBC的III期臨牀試驗。在美國,公司亦預計於獲得FDA的IND批准后啟動單藥或聯合治療骨肉瘤及乳腺癌的I/II期臨牀試驗。
海西新葯錨定的市場空間還是很有想象空間的。招股書顯示,全球乳腺癌藥物市場由2018年的242億美元穩步增長至2024年的572億美元,複合年增長率達到驚人的15.4%。預計該市場將於2032年達到886億美元,複合年增長率為5.6%。
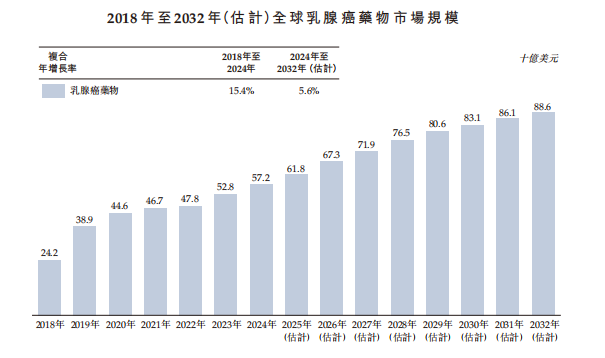
值得關注的是,公司創新葯開發進程較為依賴仿製藥的放量。現階段,雖然仿製藥銷售推動了海西新葯業績增長,但規模體量還是難以應對長期持久的新葯研發。
而且,公司的經營模式也呈現出「由輕轉重」的趨勢。據悉,海西新葯正在福州建設自有製造設施,總建築面積約9萬平方米。隨着重資產運營傾向越來越明顯,海西新葯的業績或出現較大波動。
綜上,海西新葯在仿製藥領域的紮實基礎和向創新葯的戰略轉型為其未來發展奠定了雙重動力。但是投資者也需審慎看待海西新葯的潛在風險,包括客户集中度高、現金流承壓以及創新葯研發的不確定性。未來,公司能否在仿製藥的穩定收入與創新葯的長期投入之間找到平衡,將成為其估值提升的關鍵。
推薦文章
美股機會日報 | 估值8500億美元!傳OpenAI最新融資規模將破千億美元;黃仁勛稱將發佈幾款世界前所未見的新芯片
美股機會日報 | 凌晨3點!美聯儲將公佈1月貨幣政策會議紀要,納指期貨漲近0.5%;13F大曝光!巴菲特連續三季減持蘋果
美股機會日報 | 阿里發佈千問3.5!性能媲美Gemini 3;馬斯克稱Cybercab將於4月開始生產
港股周報 | 中國大模型「春節檔」打響!智譜周漲超138%;鉅虧超230億!美團周內重挫超10%
一周財經日曆 | 港美股迎「春節+總統日」雙假期!萬億零售巨頭沃爾瑪將發財報
從軟件到房地產,美國多板塊陷入AI恐慌拋售潮
Meta計劃為智能眼鏡添加人臉識別技術
危機四伏,市場卻似乎毫不在意

