熱門資訊> 正文
中金:細胞治療開啟腫瘤免疫療法新時代
2022-02-28 08:25
- 傳奇生物(LEGN) 0
- 亘喜生物(GRCL) 0
炒股就看金麒麟分析師研報,權威,專業,及時,全面,助您挖掘潛力主題機會!
近年來以CAR-T療法為主的細胞治療已獲批上市,進入商業化兑現時期,多款潛在重磅血液瘤療法即將在美國或中國獲批,實體瘤療法也在近期公佈臨牀數據,引發行業熱度。對此,我們重點對免疫細胞療法包括CAR,TIL,TCR-T的技術發展、臨牀進度和未來關注方向進行了梳理。
多款免疫細胞療法相繼上市,行業進入迅速爆發期。自2017年首個CAR-T產品獲批以來,免疫細胞療法獲批上市速度呈加速趨勢,包括治療B細胞血液瘤和多發性骨髓瘤的CAR-T療法,以及治療葡萄膜黑色素瘤的TCR-T療法。CAR-T療法市場規模逐年增加,2021年全球銷售額已超十億美元。基於突出的治療效果及潛在市場空間,近年來商業化合作和收併購交易頻繁。
細胞治療技術和生產壁壘較高,目前更多受限於產能而非市場。細胞治療並非像小分子或抗體一樣是單一藥物成分,研發需要基礎生物學、基因工程、製藥工程,臨牀科學等多方面專業技能和經驗積累,不同公司擁有獨特的技術平臺和專利。已獲批的細胞療法均為自體產品,需要根據每位患者量身定製,生產過程複雜且不能量產,目前針對血液瘤存量患者市場,多款CAR-T產品仍處於供不應求階段。
CAR-T療法正向前線血液瘤、實體瘤和通用式療法推進,潛在市場空間廣闊。已獲批的CAR-T療法迅速開展前線血液瘤臨牀試驗,已經獲得積極數據。多款出色的多發性骨髓瘤CAR-T療法也將在近期申報上市,有望成為重磅療法。實體瘤將是細胞治療未來的主要挑戰,TCR-T和TIL治療黑色素瘤已經接近或者獲批上市,CAR-T在末線胃癌已經公佈初步有效性數據。通用式細胞療法將是未來商業化放量的關鍵,對此已有多家公司針對各種免疫細胞療法進行佈局。我們認為未來細胞療法有希望誕生出多款重磅藥物,開拓較大的腫瘤免疫市場。
風險
藥物臨牀開發時間長成本高,結果存在風險,試驗進度和報批不達預期,商業化銷售不達預期,製藥行業改革或監管可能帶來的意外影響,以及技術升級迭代風險。
細胞治療多樣化發展,CAR-T療法引發市場熱度
細胞治療是指採用生物工程的方法獲得具有特定功能的細胞用於治療疾病。細胞通過體外擴增、特殊培養等處理后,具有增強免疫、殺死病原體和腫瘤細胞、分化修復或代替病變細胞組織等功能。
圖表1:細胞治療發展歷程
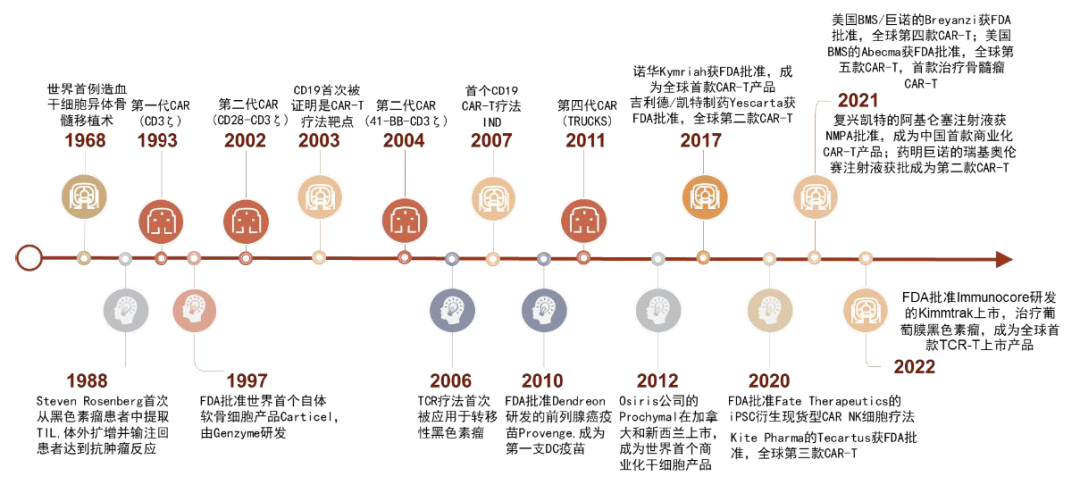
自1968年首例造血干細胞移植,細胞治療近三十年來才迅速發展,根據不同細胞來源和工程改造方式可分為免疫細胞治療和干細胞治療,由於篇幅所限,本篇重點分析免疫細胞療法。
► 免疫細胞治療指在體外對某些類型的免疫細胞如T、NK、DC細胞等進行基因工程改造或活化增殖后再輸回人體內,利用改造后加強的腫瘤殺傷力或清除病毒等功能。其中CAR-T療法經歷了超過20年研發才成功應用於臨牀,開啟了免疫細胞療法時代。
► 干細胞療法是指把健康的干細胞移植到患者體內,從而修復病變細胞或再建正常的細胞或組織。干細胞為一些細胞組織損傷不可逆的疾病提供了新的治療方式,臨牀中多用到造血干細胞、神經干細胞、皮膚干細胞、胰島干細胞等。
自2017年首款CAR-T產品Yescarta獲批后,多種CAR-T療法相繼獲批上市,因其治療血液瘤出色的療效收到廣泛關注,免疫細胞治療領域也開始迅速發展。2022年1月26日,FDA批准首款TCR-T療法Kimmtrak上市治療葡萄膜黑色素瘤,驗證了細胞治療應用於實體瘤。
美國已經有5款CAR-T上市,均治療血液瘤。其中4款靶向CD19,治療后線B細胞血液瘤,在ALL、DLBCL等病情進展迅速的血液瘤中ORR高達70-80%,在惰性FL中ORR接近100%,且療效較為持久。另一款藍鳥生物/BMS的BCMA CAR-T abecma治療末線多發性骨髓瘤,為經歷了多次化療和CD38單抗治療的患者提供了新的治療方案。這在很大程度上激勵了后續細胞治療的研發,BCMA成為CAR-T治療骨髓瘤的熱門靶點。現在傳奇生物/強生的BCMA CAR-T正等待FDA批准,其療效和安全性較abecma又進一步提升,同時臨牀往新發和前線骨髓瘤患者推進。
圖表2:獲批上市的CAR-T療法
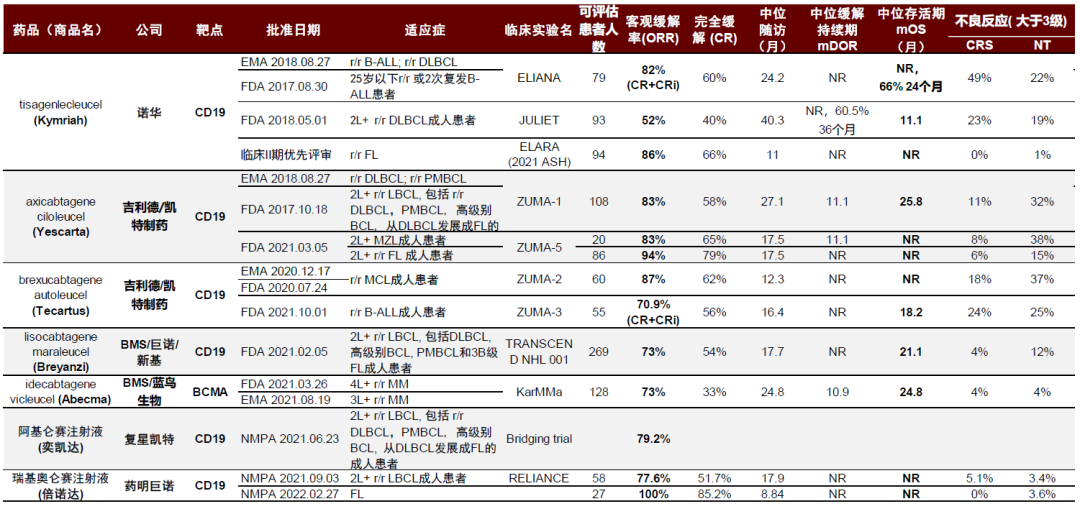
註釋:B-ALL,急性B淋巴細胞白血病;DLBCL,瀰漫大B細胞淋巴瘤;FL,濾泡性淋巴瘤;LBCL,大B細胞淋巴瘤;PMBCL,原發縱隔B細胞淋巴瘤;BCL,B細胞淋巴瘤;MZL,邊緣區淋巴瘤;MCL,套細胞淋巴瘤;MM,多發性骨髓瘤
資料來源:公司公告、FDA、EMA、NMPA、中金公司研究部
現有CAR-T療法的成功激發了市場對免疫細胞療法的熱情,成為治療癌症的新選擇,細胞治療因其獨特的作用機制,比傳統藥物有望帶來更加優異以及長期的療效。
► 在難治性和複發性晚期血液瘤中的有效性和高靶向性。基因工程改造后的細胞帶有高表達腫瘤相關或特異性抗原,在體外刺激擴增后進入患者體內,可以主動遷移到靶組織或靶細胞內發揮作用,擴大免疫應答。
► 細胞治療是「living drug」可以長時間發揮效應。細胞在體內可持久存活,腫瘤復發時立刻識別並攻擊癌細胞。現有CAR-T療法在B細胞惡性血液瘤中的mOS可長達兩年以上。首例接受治療的患者隨訪研究表明,治療后超過十年沒有檢測到白血病,體內仍可檢測到當年輸入的CAR-T細胞存在。
► 細胞治療完成后無需服藥。與傳統小分子或抗體藥物需要每月甚至每周每天服藥不同,CAR-T療法雖然早期療程複雜需要耗時1-2個月,但僅需單次細胞回輸完成治療。相比治療早線血液瘤常用的干細胞移植,CAR-T治療后也無需長期服用免疫抑制療法。
細胞療法成為熱點研發領域,現在商業化產品以CAR-T為主,在2021全球銷售額已超過十億美元,市場規模飛速增長。2022年1月Immunocore TCR-T療法Kimmtrak治療轉移性葡萄膜黑色素瘤已經獲批上市,Iovance TIL治療晚期黑色素瘤也已經報批FDA BLA,細胞療法治療實體瘤已經開始步入商業化。同時CAR-T正向前線血液瘤推進,並探索應用於胃癌等多種實體瘤。
據沙利文預計,新細胞療法的上市將會催生近百億美元市場。美國市場由商業醫保支付體系支撐,將貢獻超過一半的全球市場份額,而中國市場也因收入水平增長和商業保險的起步逐漸增加銷售額,2025年沙利文預計CAR-T全球市場可達90億美元。
圖表3:CAR-T療法全球銷售額
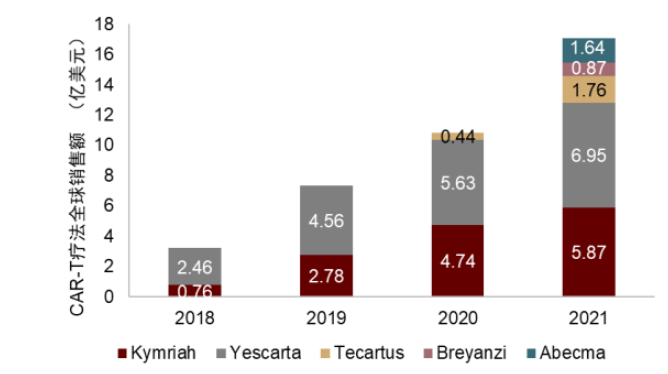
圖表4:CAR-T療法市場規模預測
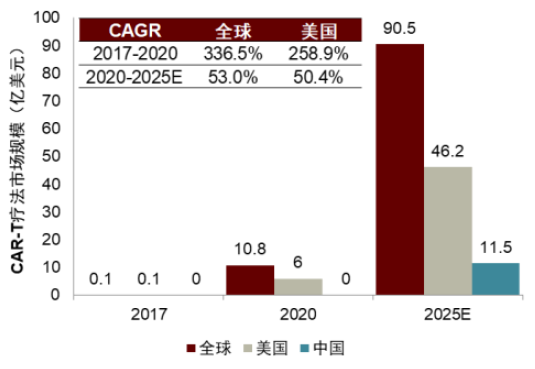
已上市的CAR-T療法效果優異且持久性較其他療法顯著改進,雖然細胞療法的市場與抗體或小分子藥物相比較小,但滿足了大量末線血液瘤患者的臨牀需求。同時CAR-T療法也面臨着諸多難題,比如實體瘤療效不佳難以突破、生產複雜繁瑣無法量產、商業化推廣困難。我們認為,細胞治療新技術若能突破這些痛點,有望拓展廣闊的腫瘤免疫市場。
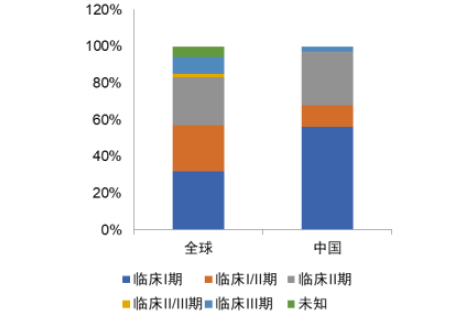
中美兩國在免疫細胞療法臨牀研發上處於全球主導地位。從種類佈局來看,中美開展了大量臨牀試驗來改進現有CAR-T療法,同時推進TIL、TCR-T、CAR-NK等新技術的臨牀試驗。從臨牀階段來看,中國在研細胞治療主要處於臨牀早期,但緊跟全球腳步快速推進國際市場。
圖表5:FDA註冊正在臨牀進行中的免疫細胞療法數量(截至2022年1月)
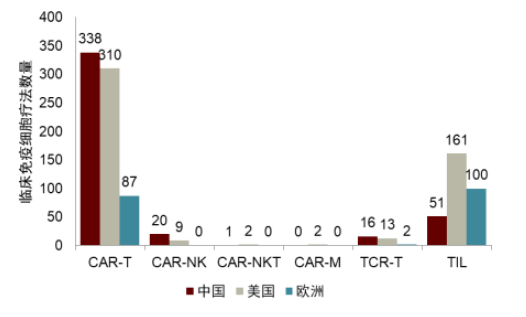
圖表6:全球和中國在研細胞治療臨牀階段分佈(截至2021年10月)
細胞治療的研發熱度也催化了多家biopharma和biotech之間的合作和收併購案例。頻繁的合作促進創新技術應用和臨牀發展,更給biotech產品商業化推廣提供了更好的平臺。
圖表7:近年國內外細胞治療主要合作併購案例

免疫細胞治療開創新一代腫瘤免疫治療
過繼性T細胞臨牀研發逐漸成熟
免疫細胞療法早期集中在利用改造后的T細胞殺傷腫瘤細胞,主要分為三類過繼性T細胞治療,包括TIL(tumor infiltrating lymphocytes, 腫瘤浸潤淋巴細胞),TCR-T(T cell receptor-engineered T cells,基因修改T細胞受體),CAR-T(chimeric antigen receptor T cells,嵌合抗原受體T細胞)療法。隨着基因工程改造方式的進步和對免疫細胞抗腫瘤特性的深入研究,近三年來CAR被應用在NK,NKT,γδT細胞等,利用這些免疫細胞的安全性、精準靶向性和多種細胞毒性等優勢,開發新一代細胞療法。
我們認為,細胞療法雖然價格高,但因療效和持久性、安全性、便捷性等優勢仍會佔有不容小覷的市場。自體或異體通用式CAR-T療法將成為末線血液瘤患者的首選,並向前線治療推進,TCR-T和自體CAR-T療法將拓寬在末線實體瘤中的應用。細胞療法雖然會與熱門靶點例如BCMA、Claudin18.2和ROR1的單抗、雙抗或ADC類藥物競爭,但仍可以互補,共同開發腫瘤免疫廣闊的市場,提高癌症患者的生活質量和治癒率。
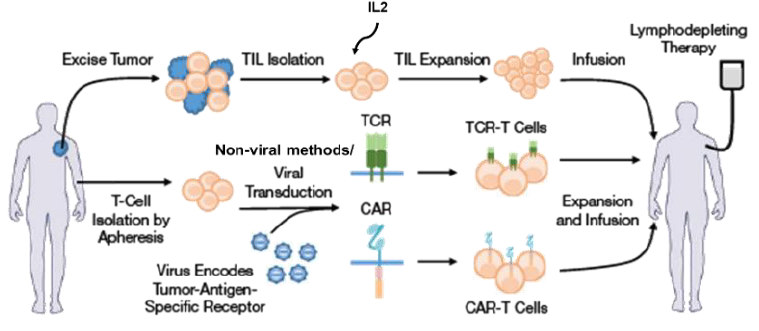
圖表8:TIL、TCR、CAR製備方法比較
圖表9:TIL、TCR-T、CAR-T特點比較
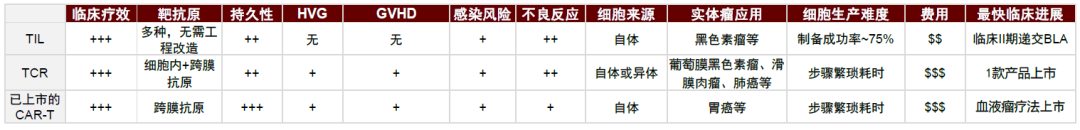
資料來源:Iovance Biotherapeutics、Immunocore、諾華、吉利德、BMS公司上市細胞療法公佈資料、中金公司研究部
CAR-T以血液瘤療為突破,現已衍生出多種療法全面進擊腫瘤免疫治療
傳統CAR-T療法經歷迭代發展不斷改進,增強技術壁壘
目前已有5款CAR-T療法獲FDA和EMA批准上市,2款獲NMPA批准上市,其中一款治療多發性骨髓瘤,其他均為B細胞血液瘤療法。CAR-T的設計是療效和安全性的關鍵,也是未來向實體瘤和通用式療法突破的難點。
CAR-T療法從患者體內分離T細胞進行基因工程改造,加入嵌合抗原受體(CAR),包含胞外抗原結合區、跨膜鉸鏈區和胞內共刺激信號區三個部分,從而激活T細胞,體外擴增后輸回患者體內,讓免疫T細胞能夠特異性地識別並殺死腫瘤細胞。
圖表10:CAR設計
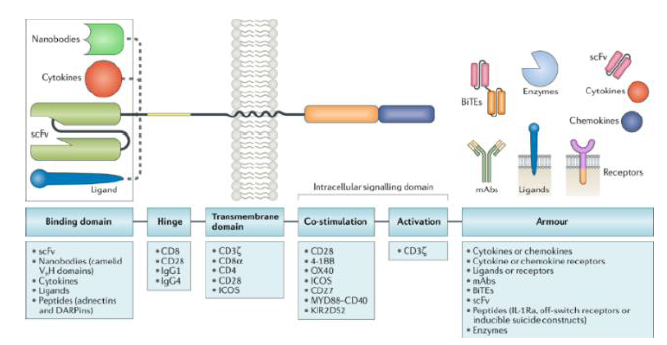
資料來源:Rafiq, Hackett, and Brentjens, 2020, Nature Reviews Clinical Oncology、中金公司研究部
圖表11:除CD19外臨牀試驗中最常見的CAR-T腫瘤抗原
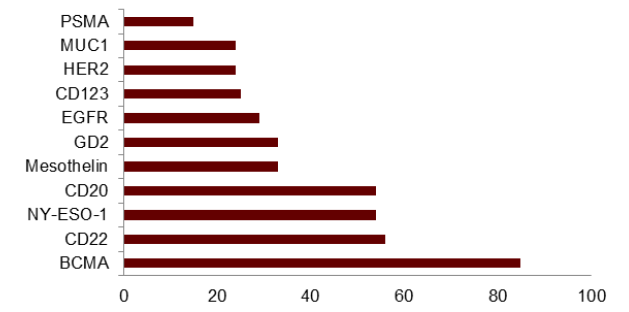
資料來源:Clinicaltrials.gov; Ivica and Young, 2021, Healthcare、中金公司研究部
► 胞外的抗原結合區負責識別並結合腫瘤特異性或相關抗原。
► 跨膜鉸鏈區的設計對CAR的性質至關重要。
► 胞內共刺激信號區的差異化設計決定了CAR-T細胞的腫瘤殺傷力和持久性,共產生了五代CAR-T。
圖表12:CAR-T療法的技術迭代設計
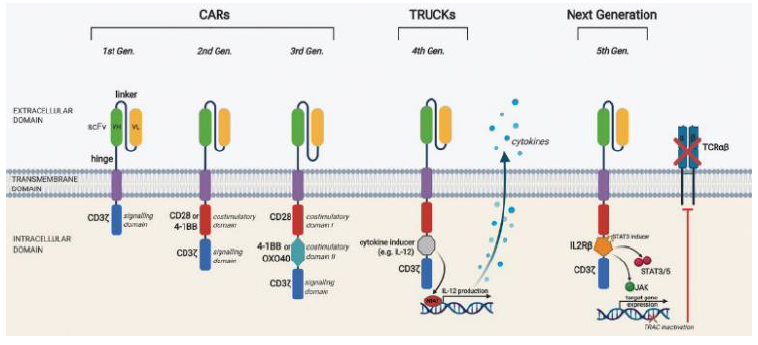
圖表13:CAR-T基於胞內共刺激信號區設計的迭代及其特點
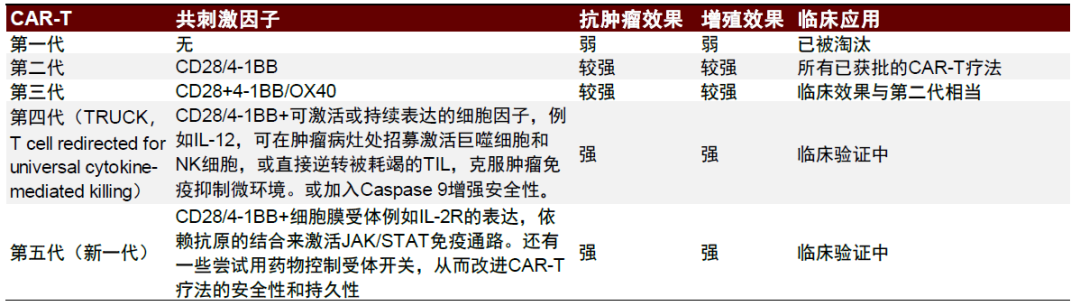
資料來源:Rafiq, Hackett, and Brentjens, 2020, Nature Reviews Clinical Oncology、中金公司研究部
CAR-T面臨治療實體瘤的挑戰
雖然CAR-T在血液瘤中效果驚艷,但在實體瘤中進展緩慢,臨牀應用前景也有諸多爭議。大多數臨牀並沒有顯示出優於現有抗體或小分子藥物的療效,因此止步於臨牀I期。目前僅科濟藥業Claudin18.2 CAR-T公佈了優秀的安全性和臨牀療效,Ib/II期初步結果顯示,在PD-1耐藥胃癌患者中ORR高達61.1%,mOS 9.5個月。這個結果增強了市場對CAR-T治療實體瘤的信心,更多藥企開始佈局針對實體瘤的早期臨牀試驗,近兩年將會有初步結果讀出。
圖表14:推進實體瘤CAR-T臨牀試驗的biotech及產品臨牀進展(截至2022年1月)
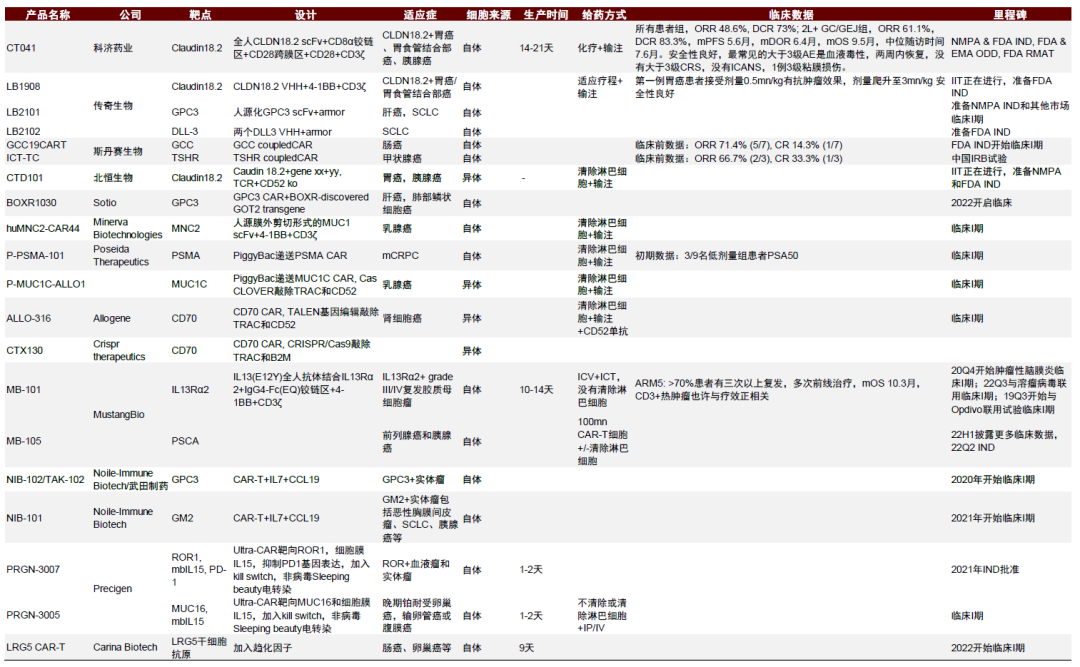
經過多年研究發現,CAR-T治療實體瘤有主要三個障礙。首先,腫瘤內部細胞抗原複雜,靶抗原選擇和CAR-T抗原結合域組合設計是一大難題,治療后容易導致靶抗原下調或者丟失,CAR-T細胞無法殺傷腫瘤。其次,CAR-T細胞運輸到腫瘤並保證其活性和穿透性也是療效不佳的限制性因素。最后,實體瘤表現複雜的是腫瘤微環境(TME),與血液瘤不同,實體瘤TME還包括浸潤性和駐留免疫細胞、基質細胞以及許多促炎和抗炎介質,相互作用複雜,多數情況下會抑制CAR-T細胞引起的抗腫瘤和免疫反應。
針對以上三個難題,大量研究投入到不同的策略來提高CAR-T細胞功能,CAR的設計是實體瘤中應用的主要壁壘。這些新一代設計的CAR-T療法多數處於臨牀前期或早期臨牀驗證,期待可以突破傳統CAR-T設計在實體瘤上的侷限。
► 從腫瘤抗原着手增強特異性。現在臨牀中CAR-T抗原選擇基本為腫瘤相關抗原,在正常組織上也有低水平表達,例如GD2,mesothelin,GPC3等。新一代基因組和蛋白組學研究着重於發現新的腫瘤特異性抗原,現在臨牀應用多是針對腫瘤相關抗原的改進,例如調節scFv或VHH的親和力,或設計可以靶向多個腫瘤抗原/腫瘤干細胞的CAR。
► 增強到達腫瘤部位的T細胞活性和浸潤冷腫瘤能力。其中一個方向是讓CAR-T細胞到達腫瘤部位再被激活,例如CAR改造成多西環素調控表達,或利用TME缺氧、synNotch受體調控表達,或表達一個靶向正常組織抗原的抑制CAR(CD19/PSMA)。另一方面是增強T細胞活性,例如增加CAR共刺激或激活區域,表達激活免疫系統的細胞因子、細胞因子受體、轉錄因子或腫瘤分泌的趨化因子,例如IL7xCCL19 CAR-T。
► 更多研究試圖直接克服抑制免疫的TME。因為實體瘤中混雜了腫瘤相關巨噬細胞(TAM),髓系來源抑制細胞,調節性T細胞和腫瘤相關成纖維細胞等。這些細胞雖然不是惡性的,但會激活腫瘤生長轉移,抑制免疫系統。因此有方法設計了成纖維細胞激活蛋白(FAP)- CAR-T,或是靶向TAM的CD123或FRβ-CAR-T,均在臨牀前展現了優秀的抗腫瘤反應。另外TME中細胞表達多種免疫檢查點蛋白。因此有方法阻斷PD-1/PD-L1來直接對抗免疫抑制反應,或表達顯性失活/細胞因子開關受體來把抑制信號轉換成生長激活信號,其中IL-4/IL-2細胞因子開關正在早期臨牀驗證中。
快速CAR-T療法改進傳統制備方法
傳統CAR-T療法生產時間至少需要兩周的體外擴增步驟,多數為人工操作,耗時且大幅增加人工和耗材成本,催生了新一代快速CAR-T療法來克服這一缺陷。
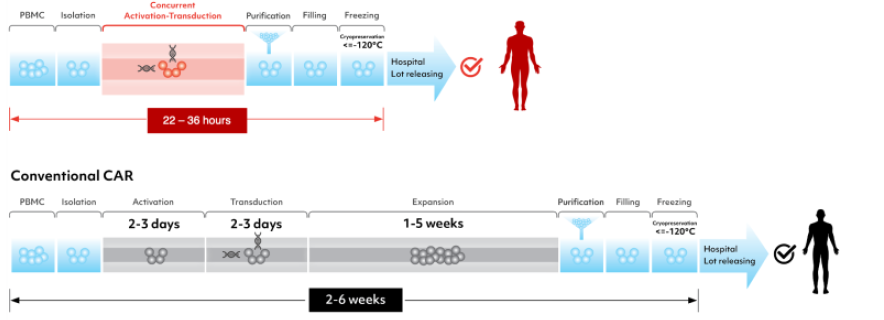
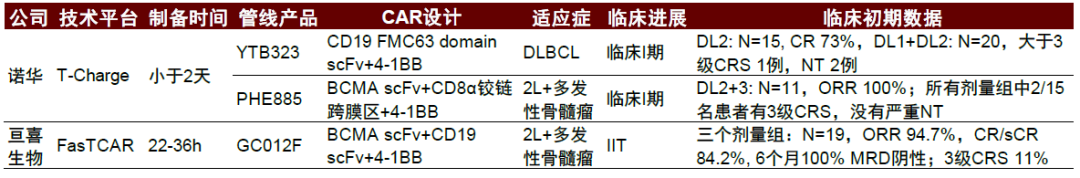
快速CAR-T療法改進了傳統自體CAR-T細胞療法的製備時間和T細胞乾性,早期臨牀展現出與傳統方法相當的安全性和有效性。諾華和亙喜生物的快速CAR-T技術平臺,可以把行業標準的2-6周製備時間縮短到2天內,CAR-T細胞轉染和激活同步進行,同時省去1-5周的體外擴增環節。這使T細胞受損程度和耗竭相應減少,強化T細胞的適應性,更好的為晚期病情迅速惡化的腫瘤患者提供了及時的治療,也可以顯著降低生產的人工和耗材成本。
圖表15:快速CAR-T與傳統制備流程比較
圖表16:快速CAR-T技術平臺臨牀進展(截至2022年1月)
異體通用式CAR-T療法成為未來細胞治療商業化量產的主攻方向
已獲批的CAR-T療法均來自患者自體T細胞,儘管有顯著的臨牀效果但限制商業化放量。傳統自體CAR-T生產複雜耗時,售價高達40萬美元或120萬元人民幣。另外,在經歷多線治療后並非所有患者自身T細胞都足夠健康可以進行改造,約5%的患者自體T細胞無法改造生產CAR-T。最后,現有CAR-T獲批的末線血液瘤惡化迅速,少數患者會在等待制備的時間中病情惡化死亡。這些問題催生了異體通用型細胞的CAR療法。
圖表17:異體通用式CAR-T療法流程
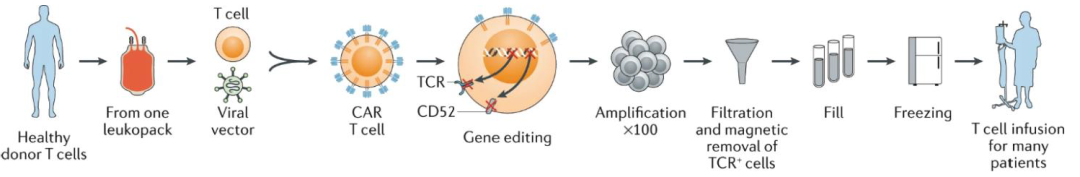
資料來源:Depil et al., 2020, Nature Reviews Drug Discovery、中金公司研究部
圖表18:主要異體通用式CAR-T技術平臺和臨牀進展(截至2022年1月)
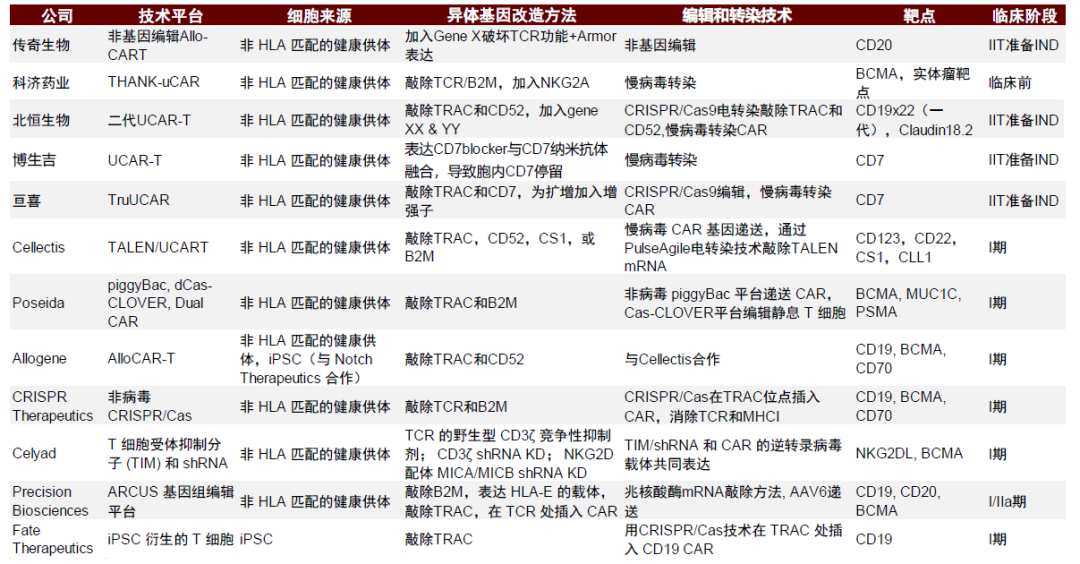
異體通用式CAR-T有三個主要優勢。第一,可以根據個體患者的既定治療方案提前生產同種異體CAR-T細胞,實現「現貨式」療法。第二,異體細胞不會經過多種抗癌治療,細胞健康狀態更好,更容易接受CAR改造。第三,小部分患者因病情和個人身體狀況很難獲得足夠的高質量CAR-T細胞,異體CAR-T療法成為更佳的選擇。因為這些優勢異體通用式CAR-T也有望能進行量產,顯著降低生產成本。
異體通用式CAR-T也面臨兩個難點。第一,異體T細胞表達的TCR會引發危及受者生命的移植物抗宿主病(GVHD)。第二,異體CAR-T細胞對於宿主免疫系統來説是外來的,受體排異反應導致被迅速清除,降低療效的持久性。
► 現在異體通用式CAR-T面臨的主要難題是體內擴增的活性和持久性,即受體排異反應(HVG)。第一種方法是採用HLA配型匹配可以有效減少排異反應。通過計算理論上分析顯示,挑選特定HLA純合體的細胞庫可以滿足超過90%患者的配型要求,然而這種方法仍比較複雜。研究發現用藥物更強效的淋巴細胞清除可以減少排異反應,但增加了感染風險[1]。現在常用的方法是敲除異體CAR-T細胞上的MHC I(B2M),因為HLA I型分子是排異反應的主導因素。但是HLA I完全缺失的細胞容易被NK細胞識別並殺死(基於missing self recognition),解決方案之一是加入HLA-E或HLA-G。
CAR-γδT拓寬了新一代異體通用療法的細胞來源
傳統CAR-T療法運用的是自體αβ T細胞,但現今也有研究聚焦在異體γδ-T細胞上,利用其不依賴MHC結合的靶細胞抗原識別特性,防止引起GvHD,更方便應用於異體通用式療法。佈局γδ-T細胞的適應症以實體瘤為主,最快進行至臨牀I期,目前來看安全性良好,有效性數據還需要更多臨牀驗證。
圖表19:γδ-T療法佈局和臨牀進展(截至2022年1月)
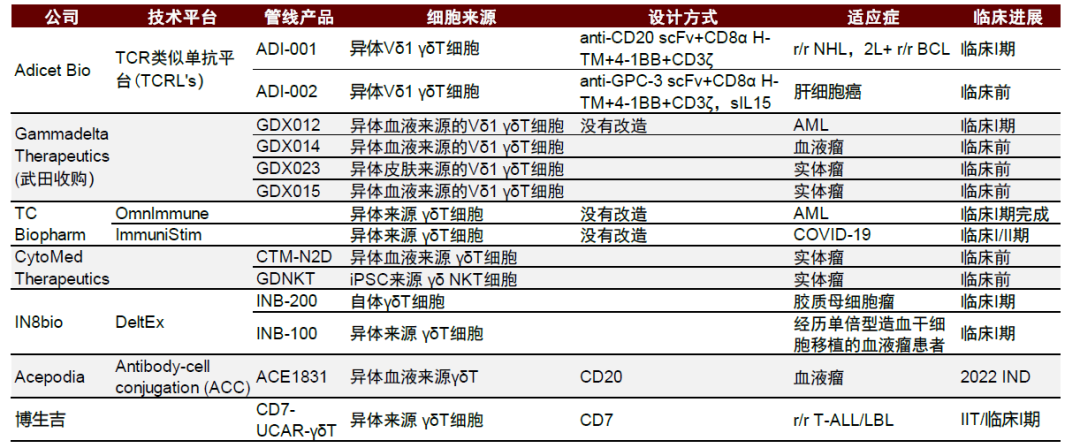
NK細胞成為異體通用免疫細胞療法熱門選擇
CAR-NK成為新一代異體通用式CAR療法的研發新方向。至今為止早期臨牀治療血液瘤和實體瘤的有效性和持久性遠遜於CAR-T療法,且需要抗體藥物聯用,多次進行清除淋巴細胞和輸注療程,但因安全性優秀,更多研發投入在改進其療效上。NK細胞是先天性淋巴細胞,具有細胞毒性效應,參與啟動適應性免疫應答,佔循環淋巴細胞15%。一旦被激活,NK細胞分泌促炎細胞因子,並觸發穿孔素、顆粒酶誘導的靶細胞裂解,具有抗癌作用。
與CAR-T相比,CAR-NK具有天然的抗腫瘤毒性和更好的通用型產品潛力。NK細胞臨牀樣本中非常豐富,來源多樣,同種異體的安全性也更好,不會引起GVHD和明顯毒性。
圖表20:CAR-NK生產流程
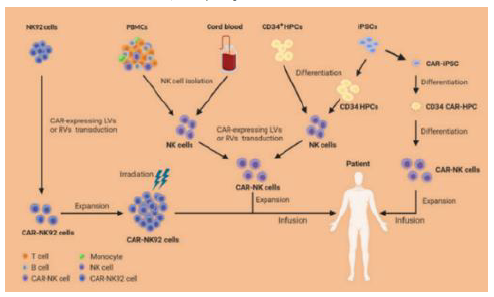
圖表21:CAR-NK療法中NK細胞來源
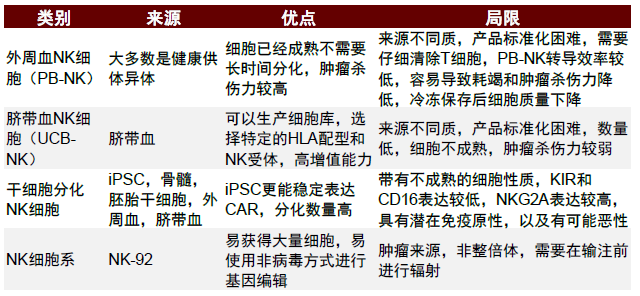
隨着基因工程技術的發展,CAR-NK設計重點集中在增強NK細胞的效力和持久性。例如針對CAR結構進行優化、運用Armored CAR(武裝CAR)加入分子有效載荷、免疫檢查點修飾克服免疫細胞耗竭等。除了NK細胞自身功能的改進外,還有些方法改善免疫抑制的TME,或者針對免疫代謝途徑進行調節,使得NK細胞更具代謝活力。
圖表22:研發CAR-NK療法的生物技術公司和臨牀進展(截至2022年1月)
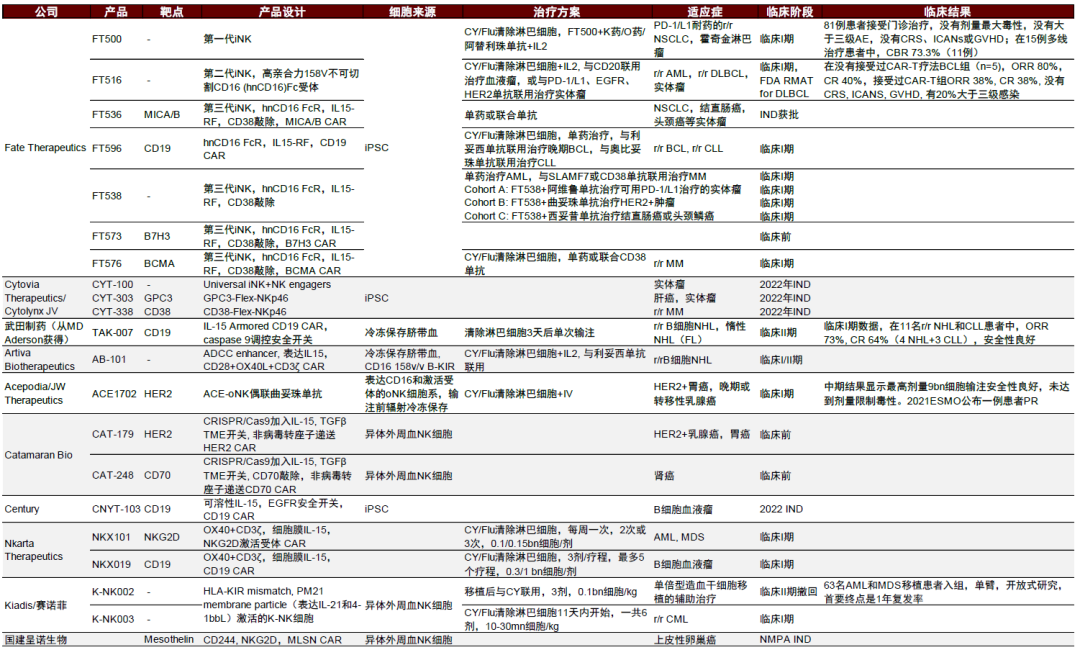
多種免疫細胞探索CAR療法
鑑於CAR-T療法的成熟和CAR-NK細胞的發展潛力,研究人員拓寬思路,開始探索CAR-NKT或CAR-M(Macrophage, 巨噬細胞)治療血液瘤和實體瘤,但臨牀結果還未成熟,需要等待未來讀出更多數據。
圖表23:佈局CAR-NKT和CAR-M的生物技術公司及臨牀進展

我們對上述總結的CAR療法進行了比較,CAR-T療法已經比較成熟,建議關注自體CAR-T療法推進前線血液瘤治療和實體瘤領域的突破,以及以異體CAR-T為主的通用式細胞療法,CAR-NK、NKT等其他免疫細胞療法尚在臨牀早期,有待更多數據驗證。
圖表24:不同細胞免疫療法比較
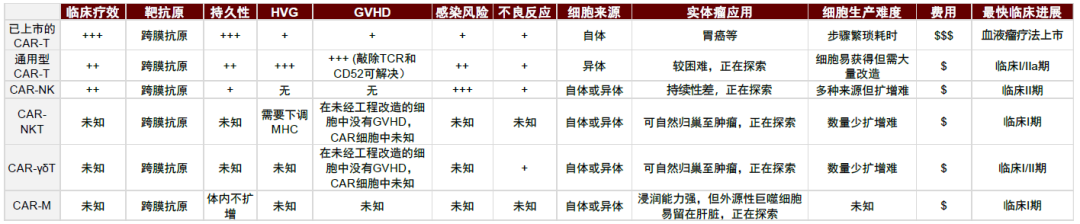
資料來源:Depil et al., Nat Rev Drug Discov, 2020、Wagner et al., Mol Therapy, 2020、Chen et al., Biomedicine & Pharmacotherapy, 2021、Xie et al., EBioMedicine, 2020、公司臨牀進展公告和會議摘要、中金公司研究部
TIL療法針對黑色素瘤有望近期上市
TIL療法從患者手術切除的腫瘤組織中純化T細胞,通過加入IL2等細胞因子刺激體外擴增腫瘤殺傷性T細胞,隨后對增殖后的T細胞進行篩選,留下對腫瘤細胞有免疫反應的克隆型,再通過將這些被擴增的T細胞輸入患者體內殺傷腫瘤細胞,適應症均為實體瘤。
TIL療法在治療末線耐藥的黑色素瘤中效果較好有望近期在美國上市,其他瘤種例如NSCLC和卵巢癌等處於I/II期臨牀有待驗證。領軍公司Iovance Biotherapeutics從TIL發現團隊Steven Rosenberg引進專利,研發的Lifileucel治療PD-1復發晚期黑色素瘤已經完成臨牀II期並申報FDA BLA。早期佈局TIL以醫院為主,例如MD安德森、Sheba醫學中心、NIH等,近年來全球佈局企業增多,例如Instil Bio、卡替醫療、沙礫生物、君塞生物、西比曼生物等,但臨牀進展較慢仍在早期。
TIL具有三點優勢:
► 腫瘤特異性強:T細胞受體多樣化,靶向多種腫瘤抗原,多靶點殺傷腫瘤組織,可克服腫瘤異質性問題。
► 靶向能力強:TIL通常由效應記憶T細胞組成,表達合適的趨化因子受體,回輸后可以更好的浸潤腫瘤組織。
► 安全性高:TIL是人體本身存在的T細胞,不經過基因工程改造,沒有免疫原性也不會與正常組織上的抗原發生交叉反應。
TIL療法也存在許多缺陷,比如該療法僅侷限於個性化治療,必須為每位患者製造特定的輸液產品,對製備生產有很高的要求,且通常超過一個月,晚期惡化快速的患者有可能因此耽誤治療。另外,從浸潤腫瘤組織中分離出特異性的T細胞操作難度很大,並且需要解決T細胞被腫瘤微環境抑制等問題,從現有數據看製備成功率不超過80%。
TCR-T利用基因工程改造TCR突破實體瘤療法
TCR(T cell receptor)是T細胞表面的特異性受體,以非共價鍵與CD3結合,通過識別並結合MHC呈遞的抗原從而激活T細胞,促進T細胞的分裂與分化。TCR-T療法提取患者或供者的T細胞並進行基因工程改造,優化TCR的親和力,使其更好地識別腫瘤抗原,在轉導至T細胞上回輸至患者體內,殺死腫瘤細胞。
TCR-T治療葡萄膜黑色素瘤2022年步入商業化階段。2022年1月26日,Immunocore宣佈Tebentafusp(Kimmtrak)獲得FDA批准,用於治療HLA-A*02:01基因型、轉移性或不可切除的葡萄膜黑色素瘤,成為首個獲批上市的TCR-T療法。Kimmtrak是一款TCR靶向gp100的通用型雙特異性TCR-scFv融合蛋白,利用ImmTAC技術平臺改造TCR提高親和力且呈可容狀態,scFv部分靶向CD3募集T細胞,在臨牀III期試驗顯示出優於選定方案的存活期和安全性。
國內外多家藥企開發了獨特的TCR-T平臺,多種實體瘤療法正在臨牀驗證中,包括治療滑膜肉瘤、NSCLC和肝癌等,靶點佈局集中在NY-ESO、MAGE-A4、GPC3等。其中Adaptimmune研發的ADP-A2M4已經申報FDA BLA,用於治療滑膜肉瘤和脂肪肉瘤。
圖表25:Kimmtrak TCR設計和臨牀III期存活率和安全性數據
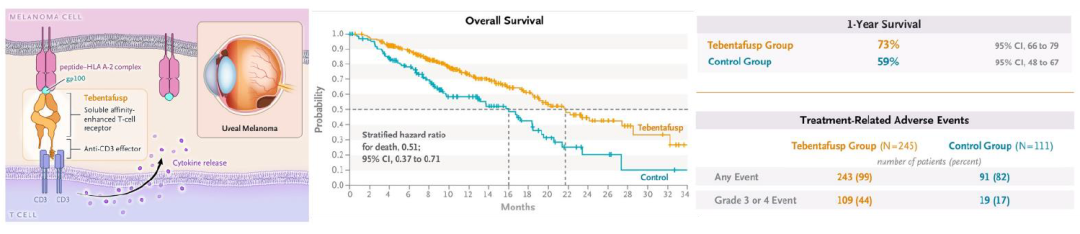
全球TCR-T療法主要佈局實體瘤,主要是因為其抗原識別和結構優勢。相比較與沒有工程改造的TIL和僅能識別靶細胞表面抗原的CAR,TCR-T是與MHC抗原複合物結合,可以對超敏感識別低水平變異的胞內抗原,適用於實體瘤在免疫抑制TME中低表達的腫瘤相關抗原。另外,TCR結構中有更多的亞單位,包括更多的免疫受體基於酪氨酸的激活基序(ITAMs),共刺激受體(CD3、CD4、CD28),對抗原依賴更小,低MHC親和力的TCR可以有效激活T細胞。
TCR-T療法已經取得了很多突破,但臨牀仍有許多要解決和優化的問題。首先是要挑選安全有效的抗原,並且篩選最佳親和力閾值的TCR,增強免疫反應的同時也要控制親和力,防止超生理的TCR親和力損傷T細胞或引發副作用。其次腫瘤免疫逃逸和TME調控仍是實體瘤細胞療法的重點難題。最后,TCR-T與CAR-T在生產原料工藝等過程中非常相似,如何降低生產成本並且提高產能也是未來商業化推廣和患者可及性的關鍵。
細胞治療目前主要壁壘:專利與生產
目前CAR-T主要的專利糾紛集中在二代CAR-T技術的共刺激區域上,包括CD28和4-1BB的專利均屬於Juno公司,其中CD28-CD3ζ CAR沒有國際專利,美國專利(US7446190)2023年失效,4-1BB-CD3ζ CAR國際專利(WO2005044996)和美國專利(US9834590)均在2024年失效,因此使用4-1BB CAR的國產CAR-T產品需要專利授權。
CAR的設計是許多biotech技術平臺差異化的根本,隨着CAR技術迭代,更多的改造方案應用到臨牀前或早期臨牀研發中,形成了較高的技術壁壘。
圖表26:CAR專利保護種類舉例

CAR的理論設計需要臨牀有效性和安全性驗證。與小分子和抗體設計可較為直接轉化為藥效不同,CAR-T細胞的改造更為複雜,例如理論上的膜外抗原結合域設計、膜內共刺激域設計、或是新一代細胞因子等設計並不一定能直接反應到CAR-T細胞對腫瘤細胞的殺傷力,尤其是在複雜的實體瘤TME,CAR的許多細節設計仍需要小鼠模型和臨牀試驗的深入驗證,產品研發中的know-how更需要大量科研經驗的團隊。
圖表27:CAR-T專利保護最多的20個靶點
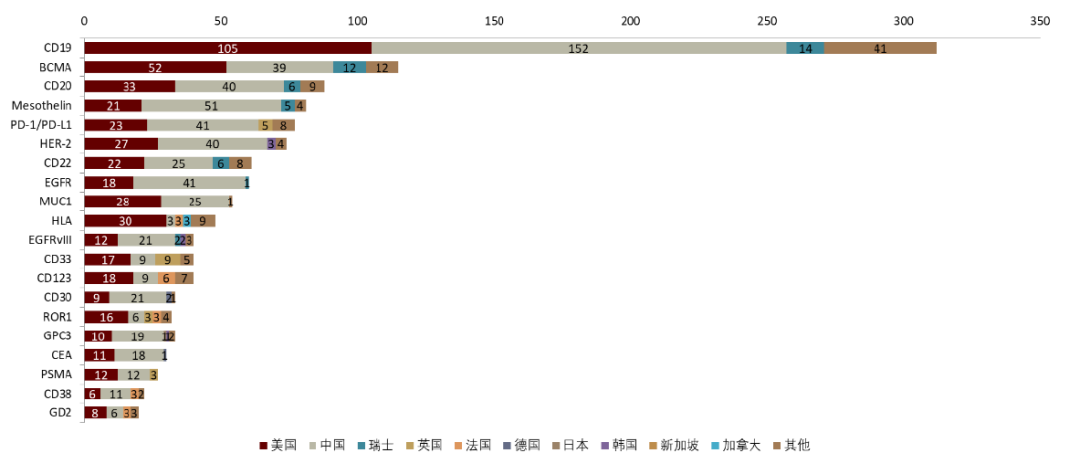
細胞治療生產過程複雜,限制商業化放量
已上市的自體CAR-T療法制備成功率隨着技術成熟可達到95%左右,但是工藝要求很高,並且細胞來源患者自體,據BMS、諾華和吉利德公佈信息,一家藥企現有的定製細胞療法產能限制約為2000-3000患者/年。製備時間上來看,諾華Kymriah工藝要求高,生產時長約20天。巨諾Breyanzi製備較為獨特,預先將CD4細胞與CD8細胞進行分離,分別轉導CAR細胞擴增,最后以1:1比例重新回輸給患者,生產時長24天左右。凱特Yescarta工藝效率較高,將生產市場縮短至17天左右,Tecartus採用了新的XLPTM生產工藝,篩選掉CD19+腫瘤細胞,減少CAR-T細胞過早激活和耗竭,提高生產成功率至96%,生產時間約為15天。
CAR-T生產環節主要涉及質粒、病毒和細胞生產,製備一份CAR-T細胞的成本約在20-50萬元,美國成本超過10萬美元,物料成本約佔70%。質粒應用於細胞治療質量控制要求高,常採用的病毒載體生產工藝難以放大且成本較高。近年來非病毒載體轉染方式,例如電轉染和轉座子的技術平臺發展有望降低開發成本。CAR-T生產耗時的關鍵步驟是細胞分選、激活、轉染、培養擴增過程,在培養細胞需要無菌環境標準化培養2-3周,增加了耗材和人工成本,且難以擴大規模。全自動、封閉式細胞生存平臺將是未來CAR-T擴大製備能力的趨勢。
圖表28:CAR-T生產流程
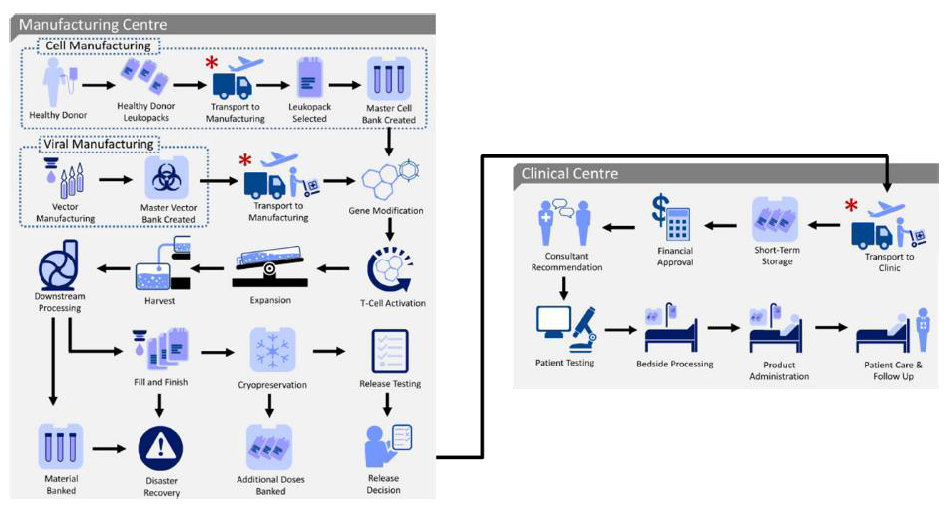
海外細胞治療更依賴於CDMO服務,外包滲透率約五成,而中國細胞治療企業傾向於自建產能。例如復興凱特的奕凱達和藥明巨諾的倍諾達生產分別來自於在上海張江和蘇州自建cGMP車間,科濟生物、傳奇生物等也有自建基地,產能建設與臨牀試驗同時推進,方便研發與生產質控,並滿足未來產品獲批上市后快速商業化需求。
由於複雜的技術機制、高門檻的工藝開發和量產限制,我們認為,未來三年限制細胞療法的商業化侷限主要為生產跟不上患者需求,尤其是血液瘤存量患者羣體較大,因此多家TIL、TCR-T、CAR-T療法的上市仍可以佔據未飽和的市場。細胞治療產業的發展也會帶來更成熟的生產操作並降低整體物料成本,並開發異體通用式等更適用於商業化量產的療法,佔據更大的腫瘤免疫市場。
國外主要細胞治療生物技術公司介紹
諾華推出首個CAR-T產品開創細胞治療先河
諾華從2012年開始與賓夕法尼亞大學開展關於CAR-T的深度合作,開發出世界首款免疫細胞治療癌症的療法CD19 CAR-T Kymriah。該款產品2017年8月首次獲得FDA批准,治療25歲以下患者r/r B-ALL,后於2018年5月FDA獲批用於治療2L+成人r/r DLBCL。2021年6月,諾華公佈Kymriah治療r/r FL的ELARA臨牀試驗優秀結果,FDA已經授予優先評審。
吉利德/凱特製藥成功商業化推廣CD19 CAR-T產品
2017年8月,吉利德宣佈以119億美元現金收購凱特製藥,獲得了凱特在研的所有CAR-T產品,使吉利德成為細胞治療領域的領跑者。Yescarta治療LBCL商業化放量快速增長,自上市以來成為銷售額第一的CAR-T產品,未來有較高潛力。
BMS佈局CD19和BCMA 兩款CAR-T療法
2019年新基被BMS收購,因此BMS獲得了新基之前在2018年收購巨諾獲得的在研CD19 CAR-T Breyanzi,也繼承了新基自 2013年起與藍鳥生物共同開發和商業化BCMA CAR-T Abecma的協議,憑藉在血液瘤商業化的優勢入局CAR-T。Breyanzi與abecma兩款產品2021年獲批,總銷售額2.5億美元,未來可能有更大增長潛力。
前凱特製藥高管成立Allogene佈局多款通用式CAR-T療法
Allogene Therapeutics由凱特製藥前高管於2017年成立,致力於開發異體通用式CAR-T療法。2018年Allogene繼承了輝瑞早前2014年與Cellectis簽訂的合作協議,獲得多款Cellectis TALEN技術平臺的UCART產品。Allogene自主開發了TurboCAR技術平臺,在Cellectis TALEN敲除TRAC和CD52的基礎上加入CAR-T-specific cytokine signal。早期臨牀數據方面,CD19 UCART 需與CD52單抗聯用來克服HVG,雖然臨牀效果難以超越自體CAR-T,但通用式CAR-T佔有生產放量和較低價格的優勢,未來商業化仍有潛力。
Fate Therapeutics引領干細胞異體CAR療法
Fate Therapeutics是行業內領先的利用多功能誘導干細胞(iPSC)平臺開發CAR療法的公司,主要專注於CAR-iNK細胞,也有一款CAR-iT細胞療法進入臨牀。Fate第二代設計了創新的高親和力、不可切割的CD16a Fc受體(hnCD16),用於增強ADCC。第三代設計增加了IL-15RF,一個用於增強細胞存活、NK細胞和T細胞激活的IL-15受體融合。另外還用CRISPR敲除CD38來防止NK細胞互相殺傷,提高代謝通路活性。第一代和第二代CAR-iNK現有數據來看有效性與其他異體通用式療法相似,安全性優秀,但需要多次注射並且與CD20單抗等聯用,給藥便利性遠低於競爭者。第三代數據有待讀出。
國內主要細胞治療生物技術公司介紹
復興凱特引進國內首個CAR-T療法
復興凱特是上海復星醫藥集團與美國凱特製藥(吉利德科學旗下公司)的合營企業,2017年在上海張江成立。復興凱特引進Yescarta進行技術轉移,並獲授權在中國進行本地化生產,2021年6月阿基侖塞注射液(奕凱達)正式NMPA獲批,治療2L+ r/r DLBCL成人患者,成為國內首款免疫細胞治療產品,售價120萬人民幣。第二個適應症2L+ r/r iNHL已獲批臨牀並被納入突破性治療藥物程序。
藥明巨諾獲批國內第二款上市CAR-T
藥明巨諾由巨諾醫療(BMS旗下公司)和藥明康德(維權)於2016年聯合創建,致力於免疫細胞治療研發,2020年11月港股上市(2126.HK)。藥明巨諾的瑞基奧倫賽注射液(倍諾達)2021年9月獲批上市,治療2L+LBCL成人患者,該款CAR-T療法以巨諾產品Breyanzi相同的CAR結構體為基礎,獲批基於RELIANCE研究評估在中國患者中的療效與安全性,數據與Breyanzi類似。倍諾達針對FL、MCL、2L LBCL等試驗也已經進入到註冊臨牀。
傳奇生物有望FDA獲批國內首款BCMA CAR-T
傳奇生物(Legend Biotech)於2014年南京成立,金斯瑞旗下子公司,后於2020年拆分納斯達克上市(LEGN.O),是國內早期研發CAR-T療法的藥企之一。其自主研發的BCMA CAR-T cilta-cel治療4L+多發性骨髓瘤臨牀數據優秀,已經與強生合作完成註冊臨牀II期試驗,2021年遞交FDA審批,PDUFA日期為2022年2月28日,同時遞交了歐洲和日本的上市申請。
科濟藥業突破CAR-T實體瘤療法
科濟藥業(Carsgen Therapeutics)成立於2014年上海,2021年6月港股上市(2171.HK),致力於CAR-T療法研發。其管線的自體Claudin18.2(CLDN18.2)CAR-T(CT041)是全球實體瘤CAR-T療法進展較快且早期臨牀結果出色的產品,也給CAR-T應用於實體瘤帶來了新的希望。CT041中國和美國報批同時進行,公司預計2022年中國遞交NDA,2023年向FDA提交BLA。公司也重點發展CMC,在中國和美國均有產能,最終希望全部自主生產。
馴鹿醫療與信達生物合作開發BCMA CAR-T
馴鹿醫療(IASO Bio)2017年成立於南京,具有全人源抗體發現和高通量CAR-T藥物優選平臺,通用式CAR-T技術平臺也在研發中。管線進展最快的為全人源BCMA CAR-T治療多發性骨髓瘤,與信達生物合作開發。馴鹿還有多款臨牀階段產品。其中CD19/CD22雙靶點CAR-T療法CT120於2021年11月被FDA授予孤兒藥資格認定(ODD),用於治療ALL。
亙喜生物開發特色快速CAR-T技術平臺
亙喜生物(Gracell Biotechnologies),2021年1月納斯達克上市(GRCL.O)。亙喜是首個推出快速製備CAR-T療法FasTCAR平臺的公司,將自體CAR-T細胞生產時間從行業標準的2到6周顯著縮短到次日生產完畢,對末線疾病惡化迅速的患者提供了更佳選擇。FasTCAR產品BCMA/CD19雙靶點CAR-T GC012F針對多發性骨髓瘤,在早期臨牀顯示出了具有競爭力的療效和安全性,公司預計2022年中美申報IND。
北恆生物研發通用式CAR-T平臺佈局血液瘤和實體瘤
北恆生物是國內首批開展的異體通用式CAR-T療法的公司之一,公司第一代UCAR平臺採用CRISPR/Cas9技術破壞TRAC和CD52,並基於此平臺開發了CD19/CD22雙靶點UCAR-T療法CTA101,用於治療r/r ALL。在第一代UCAR平臺的基礎上北恆生物開發了新一代UCAR,自主專利加入了兩個基因表達,增強T細胞的擴增和TME的浸潤,基於此平臺的Claudin18.2 UCAR-T正在進行IIT並準備中美IND申報。
斯丹賽生物:2009年在上海成立,自主研發CoupledCAR技術平臺治療實體瘤。GCC19CART治療r/r結直腸癌已獲FDA IND,2022年開展臨牀I期。
博生吉醫藥科技:2010年在蘇州成立,擁有Safeγ UCAR-γδT平臺、CAR結構功能驗證平臺、全自動CAR-T製備平臺等。多款異體通用式CAR-T、CARγδT和CAR-NK細胞產品正在臨牀前研發。臨牀進展最快的是自體CD7 CAR-T療法PA3-17,用於治療T-ALL已經獲批NMPA IND,處於臨牀I期。
西比曼生物科技:2011年在上海成立,擁有多款管線產品,其中C-CAR088 BCMA-CAR-T治療多發性骨髓瘤,C-CAR039 CD19/CD20 CAR-T治療r/r NHL(獲得FDA ODD),AFP TCR-T治療肝細胞癌,TIL1與PD-1聯用治療NSCLC正處於臨牀I期試驗。公司也在干細胞療法方面有所佈局,利用人脂肪組織來源間充質祖細胞治療關節和自身免疫疾病。
藝妙神州:2015年在北京成立,IM19自體CD19 CAR-T治療DLBCL, B-ALL與MCL正在國內臨牀I期試驗,公司也與博雅輯因合作開發異體CAR-T產品。
優卡迪生物醫藥科技:2015年在上海成立,擁有siRNA調控的SMART技術平臺和優化抗體的MADDS技術平臺。其中自體CD19 CAR-T產品U01針對BCL中樞神經系統白血病處於國內臨牀I期。公司也佈局了自體和異體的實體瘤CAR-T療法研發。
合源生物科技:2018年在天津成立,CNCT19 自體CD19 CAR-T治療ALL和NHL正在國內臨牀I期試驗。
風險
► 臨牀藥物開發時間漫長,成本較高,結果存在不確定性,相關公司可能無法按計劃完成候選藥物的臨牀試驗。
► 臨牀試驗進展和藥品審批可能延期或不及預期。
► 相關公司候選藥物的商業銷售盈利情況受原料供給、產能限制、市場波動等因素影響可能會不及預期。
► 製藥行業改革或監管可能給相關公司帶來
意外影響。
► 技術升級迭代導致競爭格局發生變化。
[1] Depil, S., Duchateau, P., Grupp, S.A. et al. ‘Off-the-shelf’ allogeneic CAR T cells: development and challenges. Nat Rev Drug Discov 19, 185–199 (2020). https://doi.org/10.1038/s41573-019-0051-2
本文摘自:2022年2月15日已經發布的《細胞治療開啟腫瘤免疫療法新時代》
何子瑜 SAC 執業證書編號:S0080518120001 SFC CE Ref:BNF440
周王濱 SAC 執業證書編號:S0080120090084
鄒 朋 SAC 執業證書編號:S0080513090001 SFC CE Ref:BCC313
推薦文章
一周財經日曆 | 壓軸登場!小米、拼多多等重磅財報來襲;深演智能、雲英谷科技等新股下周上市;港美股下周一休市一日
港股周報 | 利好共振!芯片股集體狂飆,兆易創新周漲超43%;阿里致股東信:將AI+雲打造成新增長動力;聯想飆漲20%刷歷史新高
美股機會日報 | 今晚11點!特朗普將親自「加冕」美聯儲新主席沃什;英偉達Vera Rubin機架售價狂飆!產業鏈所有組件迎漲價熱潮
SpaceX在發現多項問題后推迟「星艦」第12次試飛
華盛早報 | 沃什今晚11點宣誓就職美聯儲主席!雷軍稱未來兩年內存或持續漲價;Q1恆指季檢結果今晚公佈
特朗普再威脅伊朗交出濃縮鈾!稱到手后或銷燬
美股機會日報 | 伊朗稱高濃縮鈾不得運往國外;特朗普再出手!美國政府20億美元佈局量子計算;SpaceX正式遞表衝刺納斯達克
一圖看懂 | 連續兩季盈利!蔚來Q1經營利潤0.66億元,交付量超8萬輛;毛利率創近四年新高

